Serhiy
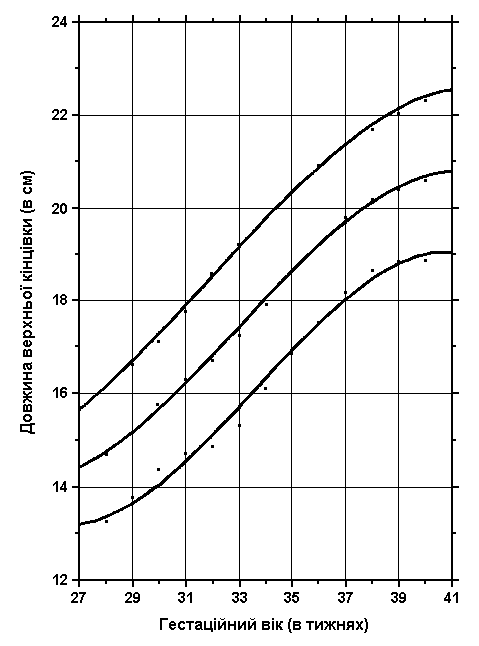
Довжина верхньої кінцівки
Із українського перекладу книги “Growth References: Third Trimester to Adulthood. Compiled by Saul RA, Geer JS, Seaver LH, Phelan MC, Sweet KM, Mills CM. Greenwood Genetic Center. 1998”.
3, 50 та 97 перцентилі довжини верхніх кінцівок відповідно до гестаційного віку. Довжина верхньої кінцівки – це відстань між акроміоном та кінчиком третього пальця витягнутої паралельно тілу руки. Дані обстеження 87 доношених (48 хлопчиків та 39 дівчаток) та 111 недоношених (55 хлопчиків та 56 дівчаток) ізраїльських новонароджених 27-41 тижнів гестації у перші 36-60 годин життя. Жодна дитина не мала вроджених вад. Merlob P et al: Birth Defects: Orig Art Series XX(7):34, 1984.
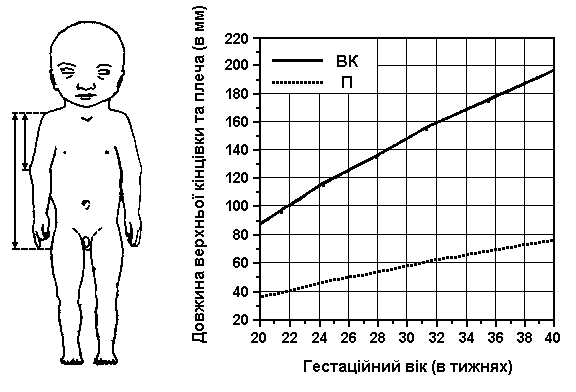
Вимірювання верхніх кінцівок
Із українського перекладу книги “Growth References: Third Trimester to Adulthood. Compiled by Saul RA, Geer JS, Seaver LH, Phelan MC, Sweet KM, Mills CM. Greenwood Genetic Center. 1998”.
За Scammon та Calkins: The Development and Growth of the External Dimensions of the Human Body in the Fetal Period, University of Minnesota, 1929.
Пентада Кантрелла
(Pentalogy of Cantrell)
Ірина Ткач
Акушер-гінеколог
Зарічненської ЦРЛ Рівненської області
Включення:
Торако-абдомінальна ектопія серця, торакоабдомінальний синдром, синдром Кантрелла, синдром Кантрелла-Геллера-Равіча, перитонео-перикардіальна діафрагмальна кила.
Визначення:
Пентада Кантрелла – це комплекс вроджених вад розвитку дизрафічного ряду. Повний синдром характеризується двома головними дефектами: ектопією серця і дефектом черевної стінки (частіше у вигляді омфалоцеле, хоча може також мати місце розходження м’язів черевної стінки). Вперше синдром описаний Кантреллом у 1958 році, спостерігається спорадично.
Основні діагностичні критерії:
Діагноз повного синдрому вимагає п’ятьох критеріїв, описаних Кантреллом, але спостерігаються і неповні форми. Дефекти грудини можуть виявлятися у вигляді відсутності мечоподібного паростка, повного розщеплення грудини, її вкорочення аж до повної відсутності грудини. Черевний дефект може бути у вигляді широкого розходження прямих м’язів живота або великого омфалоцеле. Найбільш поширені інтракардіальні вади проявляються у вигляді міжпередсердних та міжшлуночкових дефектів і тетради Фалло.
Відносно частоти аномалій, що зустрічаються при синдромі Катрелла, то абдомінально-стернальні дефекти зустрічаються в 74,5%; омфалоцеле в 59,4%; дефект діафрагми в 56,8%; дефект перикарда в 41,8%. Що стосується серцевих аномалій, то вони зустрічаються з частотою 83%, з них найчастіше відслідковуються інтравентрикулярні дефекти, дивертикул шлуночка, шлуночкові аневризми, стеноз легеневої артерії, декстрокардія, аномальне впадіння верхньої порожнистої вени, аномальне відходження легеневої артерії та відкрита артеріальна протока, інколи тетрада Фалло.
Рентгенівське дослідження може виявити дефекти грудини, декстрокардію та інші відхилення.
Магнітно-резонансна томографія дає можливість підтвердити наявність тих чи інших аномалій, а також дослідити серцево-судинну гемодинаміку.
Асоційовані аномалії:
Є повідомлення і про інші дефекти, а саме: розщілину піднебіння і губи, кистозну гігрому, клишоногість, вади формування грудини, транспозицію великих судин, відкриту артеріальну протоку, дефекти міжшлуночкової перегородки, дивертикул лівого шлуночка, гіпоплазію легень, мальротацію, гідроцефалію, аненцефалію, гіпоспадію та інші.
Диференційний діагноз:
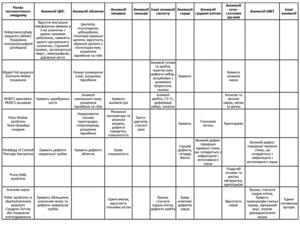
Диференційний діагноз слід проводити з ізольованою ектопією серця, ізольованим дефектом черевної стінки, ізольованим омфалоцеле, ізольованою тетрадою Фалло та іншими патологічними станами, викладеними у таблиці 1.
Етіологія:
Невідома. Іноді пов’язується з хромосомними аномаліями. Описані асоціації синдрому з трисомією 18, трисомією 13 і синдромом Тернера. Є дані, які підтверджують виникнення хвороби при успадкуванні Х-зчепленого гену (генний локус Xq25-q26.1).
Патогенез:
Основною причиною є порушення, пов’язане з розвитком сегменту мезодерми між 14 і 18 днями після запліднення, коли вісцеральна і корпоральна мезодерми розділяються. Грудна, черевна стінка, перикард і частина діафрагми є похідними мезодерми тіла, у той час як міокард є результатом поділу клітин органної мезодерми. Бічні мезодермальні клітини мігрують до серединної лінії зародкового диска і змикаються попереду. Якщо цього не відбувається, то залишаються дефекти черевної стінки, грудини, діафрагми і перикарду.
Порушення під час розподілу мезодерми призводять до порушень, які вкладаються в пентаду Катрелла.
Поширеність:
Дуже рідкісний. Зустрічається спорадично. Менше, ніж про 90 випадків було повідомлено в літературних джерелах. Зустрічається, за даними літератури, з частотою 5,5 випадків на 1 млн. живонароджених, причому переважно у чоловічої статі.
Пренатальна діагностика:
Можливість виявлення даних аномалій при сонографічному дослідженні залежить від вираженості, величини та сукупності вад.
Навіть при народженні встановити повну ступінь синдрому важко, оскільки дефект грудини може бути незначним і без істинної ектопії серця.
Прогноз:
За даними літератури відомо про виживання в 20% випадків. Це стосувалось випадків з помірними дефектами і неповним вираженням синдрому.
Повний прогноз здається несприятливим і цілком залежить від величини стернальних та вентральних дефектів.
Лікування:
Після народження дитини втручання з приводу ліквідації омфалоцеле не повинно відтягуватись. Відновлення дефектів грудини, діафрагми та перикарду може бути проведене одночасно.
Часто хірургічне втручання виконати важко або взагалі нереально внаслідок гіпоплазії грудної клітки і неможливості ліквідувати ектопію серця. Деякі новонароджені мають виражену дихальну недостатність, часто вторинну внаслідок легеневої гіпоплазії. Розпізнавання й ліквідація будь-яких інтракардіальних вад важливі, оскільки вони є основною причиною смерті в постнатальному періоді.
Номер з каталогу МІМ:
313850 Thoracoabdominal Syndrome; THAS.
Література:
- Пренатальная диагностика врожденных пороков развития плода /Р. Ромеро, Дж. Пилу, Ф. Дженти, А. Гидини, Дж.С. Хоббинс.- М.: Медицина.- 1994.- C. 222-223.
- Benacerraf BR. Ultrasound of fetal syndromes. Churchill Livingstone 1998:267-269.
- Thoracoabdominal Syndrome. OMIM #313850.
Переглянуто редакційною колегією I.B.I.S.: 27/08/2003
Нирковий канальцевий синдром Фанконі
(Fanconi Renotubular Syndrome)
Людмила Зайцева
Лікар–неонатолог
Волинського обласного дитячого територіального медичного об’єднання
Синоніми:
- Нирковий Фанконі синдром;
- Фанконі синдром дорослих;
- Фанконі синдром без цистенозу;
- Людер-Шелдона синдром.
Основні діагностичні критерії:
- Гіпофосфатемічні пошкодження скелету;
- Генералізована аміноацидурія;
- Ренальна глюкозурія.
Тип успадкування:
Аутосомно-домінантний. Експресивність мутантного гена в гомозиготному стані значно варіює, зустрічаються спорадичні мутації.
Генне картування: 15q15.3.
Патогенез:
В основі генетично обумовлені дефекти ферментативного фосфорилювання в ниркових канальцях. Як наслідок, виникає порушення процесів енергозабезпечення транспорту фосфорів, глюкози, амінокислот, підвищена екскреція останніх з сечею та порушення рівноваги кислот та основ. Метаболічний ацидоз і недостатність фосфорних сполук викликають порушення кісткової тканини по типу остеомаляції і рахітоподібних змін скелету.
Патоморфологія:
Укорочення та звуження проксимального канальця у вигляді лебединої шиї, дегенерація, атрофія тубулярного епітелію.
Клінічні симптоми:
- Глюкозурія, аміноацидурія, протеінурія, лактоацидурія;
- Гіпофосфатемія, гіпокаліємія;
- Ацидоз;
- Рахіт, остеомаляція;
- Затримка росту, м’язова слабкість;
- Ниркова недостатність.
Диференційна діагностика:
- Рахіт;
- Остеопатії;
- Нефротичний синдром при трансплантації нирок;
- Амілоідоз;
- Гіпопаратиреоз;
- Ураження нирок солями важких металів;
- Отруєння лікарськими речовинами.
Обстеження:
Рентгенологічно-системний остеопороз, розрідження зон росту, відставання темпів росту кісткової тканини від біологічного віку.
Лікування симптоматичне:
- Лужна терапія з метою корекції ацидозу під контролем РН крові;
- Введення електролітів, таких як сода, фосфати, кальцій, магній;
- Лікування вітаміном Д повторними курсами (початкова добова доза вітаміну Д 25-30 тисМО, максимальна – 75-150 тисМО);
- Вітаміни А, С, Е, група В;
- Дієта з обмеженням солі, багата на кальцій;
- У фазі ремісії – масаж, соляно-хвойні ванни;
- Хірургічна корекція можлива при розвитку важких кісткових деформацій на фоні досягнення стійкої клініко-біохімічної ремісії протягом 2-х років.
Прогноз: залежить від основного захворювання.
Номер з каталогу МІМ:
134600 Fanconi renotubular syndrome.
Література:
- Ben-Ishay, D.; Dreyfuss, F.; Ullmann, T.D.: Fanconi syndrome with hypouricemia in an adult: family study. A. J. Med. 31: 793-800, 1961.
- Brenton, D. P.; Isenberg, D. A.; Cusworth, D. C.; Garrod, P.; Kryvavych, S.; Stamp, T.C.B.: The adult presenting idiopatic Fanconi syndrome. J. Bone Joint Surg.38B: 204-226, 1956.
- Dent, C. E.; Harris, H.: Hereditary form of rickets and osteomalacia. J. Bone Joint Surg. 38B: 204-226,1956.
- Friedman, A.L.; Trygstad, C.W.; Chesney, R.W.: Autosomal dominant Fanconi syndrome with early renal failure. Am. J. Med. Genet. 2: 225-232, 1978.
- Lichter-Monecki, U.; Broman, K. W.; Blau, E.B.; Konecki D.S.: Genetic and physical mapping of the locus for autosomal dominant renal fanconi syndrome, on chromosome 15q15.3. Am. J. Hum. Genet. 68: 264-268, 2001.
Переглянуто редакційною колегією I.B.I.S.: 09/09/2003
Синдром Казабаха-Мерріта
(Kasabach-Merritt Syndrome)
О.В. Мурінець
Лікар–неонатолог
Міського пологового будинку №2, м. Сімферополь
Визначення:
Феномен, який характеризується поєднанням прогресуючої гігантської гемангіоми та тромбоцитопенією. Захворювання докладно описане у 1940 р. H.H. Kasabach і K.K. Merrit. Феномен Казабаха-Мерріта описаний, як рідкісне ускладнення у дітей з поширеними судинними новоутвореннями.
Співвідношення статей: Ж1 : Ч1.
Етіопатогенез:
Спадкового характеру не встановлено. Проявляється у ранньому віці. Процеси, які відбуваються в гемангіомі, за механізмом є хронічною формою ДВС-синдрому. У велетенській гемангіомі, яка має розгалужену судинну мережу, відбувається уповільнення кровообігу з утворенням великої кількості мікротромбів та підвищеним використанням тромбоцитів. В результаті цього розвивається вторинна (набута, симптоматична) тромбоцитопенія та коагулопатія споживання, пов’язана з підвищенням зсідання крові в гемангіомі. Тромбоцитопенія сприяє зниженню продукції тромбоцитів, оскільки відбувається функціональне виснаження резервів, пов’язане з постійним підвищеним руйнуванням тромбоцитів у гемангіомі. Сучасними дослідженнями доведений зв’язок з такими рідкісними судинними новоутвореннями як “kaposiform gemangioendothelioma” і вроджена “tufted angioma”.
Клініка:
Зазвичай клініка явно розвивається у перші місяці життя (у ранньому грудному віці), але часом має місце пізній початок. Гемангіоми часто виявляються уже при народженні, вони характеризуються значними розмірами і, як правило, поодинокі, однак, множинні невеликі гемангіоми також можуть бути причиною тромбоцитопенії.
Судинні ураження локалізуються на шкірі тулуба, кінцівок, рідко на обличчі; їх відрізняє швидкий ріст. Рідше можуть знаходитися у кістках скелету, головному мозку, органах черевної порожнини. Порушення, пов’язані з тромбоцитопенією, приводять до спонтанних кровотеч, які супроводжуються екхімозами, петехіями та швидким збільшенням розміру гемангіоми. При важкій тромбоцитопенії можуть виникати кровотечі зі слизової оболонки носової порожнини, шлунково-кишкового тракту з наступним розвитком важкої анемії.
Лабораторна діагностика:
У периферичній крові виявляють тромбоцитопенію, фрагментовані еритроцити, постгеморагічну анемію, іноді анемія може мати гемолітичний характер. У кістковому мозку визначається адекватна чи збільшена кількість нормальних або незрілих мегакаріоцитів. Час кровотечі подовжений, порушується ретракція кров’яного згустка, має місце гіпофібриногенемія, зниження факторів зсідання 2, 5, 7 і 8 та їх виснаження. Може виявлятися збільшена кількість продуктів розщеплення фібрину, як показник коагулопатії споживання. Тривалість життя тромбоцитів і еритроцитів також скорочена.
Патанатомія:
Судинна пухлина, яка має кавернозну будову і складається з великої кількості порожнин, заповнених кров’ю. Тромбоцити потрапляють у “пастку” розгалуженого судинного русла пухлини, в якому і руйнуються.
Лікування:
Терапія синдрому Казабаха-Мерріта здійснюється у двох напрямках. Консервативна терапія гострого періоду спрямована на зупинку кровотечі та підтримку життєдіяльності організму. Проводять трансфузії крові, тромбоцитарної маси, використовують симптоматичні засоби. Оскільки кортикостероїди можуть прискорити інволюцію гемагіоми, виправдане проведення пробного курсу лікування ними, особливо у немовлят. Гормональна терапія також показана при передопераційній підготовці.
Позитивний ефект дає променева терапія (одноразове опромінення у дозі 600-800 рад), яка призводить до зменшення гемангіоми та геморагічних проявів, однак може з’явитися необхідність у повторних курсах.
При певних анатомічних умовах може бути здійснене зовнішнє стискання пухлини чи радикальне видалення її, але хірургічне лікування може призводити до неконтрольованої кровотечі. Спленектомія неефективна та протипоказана.
Прогноз:
Захворювання досить серйозне. Спонтанний тромбоз гемангіоми може привести до облітерації судин і спонтанного видужання. Прогноз серйозно ускладнюється при кровотечах у життєво важливих органах.
Номер з каталогу МІМ:
141000 Hemangioma-Thrombocytopenia Syndrome.
Література:
- Гематологические болезни у детей.- Минск, 1996.- C. 163.
- Керпель-Фрониус Э. Педиатрия.- Будапешт, 1975.- C. 542-543.
- Педиатрия /Под ред. Р. Е. Берман, В. К. Воган.- 13 изд.- Kн. 7.- C. 237-238.
- Шабалов Н. П. Неонатология.- СПб, 1995.- T. 1.– C. 464.- T. 2.- C. 164.
- Diseases of the newborn. Taeusch, Ballard, Avery. 6th edition:1000-1001.
- Nelson Textbook of Pediatrics. Editors: Vaughan III VC, McKay Jr RJ, and Behrman RS. 11th edition. 1979:1417-1418,1867.
- Polin RA, Spitzer AR. Fetal and neonatal secrets. 2001:83.
Переглянуто редакційною колегією I.B.I.S.: 19/03/2003
Фетальний цитомегаловірусний синдром (ЦМВ)
(Congenital Cytomegalovirus Syndrome)
О. Тарасюк
Лікар акушер–гінеколог
Березнівської центральної районної лікарні Рівненської області
Основні діагностичні критерії:
- Гепатомегалія;
- Спленомегалія;
- Петехії;
- Тромбоцитопенія;
- Довготривала жовтяниця новонароджених;
- Пневмонія;
- Затримка росту;
- Мікроцефалія;
- Кальцифікація головного мозку.
Дані обстежень:
- Пренатальна УЗД:
- Синдром затримки розвитку плода;
- Аномальна кількість навколоплідних вод;
- Порушення структури плаценти (варикозне розширення її судин, наявність гіперехогенних включень, набряк плаценти, контрастування базальної пластини);
- Ознаки передчасного чи запізніле дозрівання плаценти;
- Неправильної форми розширення міжворсинчастого простору, що не відповідають центрам котилідонів;
- Рання поява дольчастості плаценти;
- Збільшення розмірів живота і розширення чашечко–мискової системи нирок плода.
- Кардіотокограма: при внутрішньоутробній пневмонії перед пологами реєструється “ніякий” тип кардіотокограми, що свідчить про внутрішньоутробну гіпоксію та низькі компенсаторні можливості плода.
- Біофізичний профіль плода:
- Зниження тонусу плода;
- Ареактивний нестресовий тест.
- Лабораторні дані:
- Виділення вірусу. Вірус може бути виділеним з амніотичної рідини, глоткового мазка чи проби сечі інфікованого малюка.
- Серологія. Виявлення ЦМВ – специфічних IgM антитіл в одиничній пробі крові вказує на недавно перенесену або наявну інфекцію. Сероконверсія в період між двома пробами крові також свідчить про наявну інфекцію.
- Проби. Антенатальні обстеження. При відсутності симптомів інфекцію у матері в період вагітності виявити практично неможливо. Виявлення первинної інфекції при вагітності можливе за допомогою лабораторного аналізу проб крові, отриманих в антенатальний період. Після первинної інфекції IgM–антитіла персистують до 16 тижнів, але цей термін може варіювати у різних людей, а також в залежності від виду лабораторного тесту. В зв’язку з цим виявлені IgM–антитіла можуть бути пов’язані з інфікуванням, яке відбувалось ще до початку вагітності. В даний час відсутній метод виявлення вагітних жінок з рецидивуючою інфекцією, котра може призводити також до внутрішньоматкової передачі інфекції.
- Обстеження плода. На даний час не існує надійної процедури для діагностики інфекції плода після того, як діагностована первинна інфекція у матері в період вагітності. Вірус може бути виділений з амніотичної рідини, а ЦМВ–специфічні IgM–антитіла можуть бути виявлені в крові плода, отриманої шляхом фетоскопії, кордоцентезу. Однак подібні процедури інвазивні, їх неможливо провести в ранньому терміні вагітності і вони пов’язані з підвищеним ризиком самовільного аборту.
- Неонатальні і постнатальні обстеження. Вроджена інфекція може бути підтверджена або шляхом виділення вірусу з глоткового мазка чи проби сечі, взятих протягом перших 3-х тижнів життя новонародженого, або шляхом виявлення ЦМВ–специфічних IgM–антитіл в крові малюка чи в крові пуповини. Зараження звичайно відбувається при народженні чи в ранньому малюковому віці. Через це неможливо поставити точний діагноз вродженої ЦМВ–інфекції ні у малюка на більш пізньому етапі, ні в дитини, навіть якщо наявні у них симптоми дозволяють запідозрити вроджену ЦМВ–інфекцію. IgM–антитіла можуть вказувати на недавно розвинуту неонатальну чи постнатальну інфекцію. Виділення вірусу в навколишнє середовище постійно відбувається у дітей як з набутою, так і з вродженою інфекцією. Однак, якщо збереглись антенатальні проби крові матері, а у малюка страшого 3-х тижнів підозрюється вроджена ЦМВ–інфекція, тоді можливо обстежувати проби материнської крові на сероконверсію чи підтвердити наявність ЦМВ–специфічних IgM–антитіл в період вагітності.
- Біологічне обстеження посліду:
- Вогнищева затримка дозрівання ворсин;
- Редукція судинного русла;
- Щільність міжворсинчастих проміжків;
- Поліморфно–ядерна інфільтрація оболонок;
- Ворсинки з витонченим хоріальним епітелієм;
- Склад форменних елементів крові в судинах плаценти;
- Склерозовані, “замуровані” у фібриноїд ворсинки.
- Проводиться також визначення геному збудника в гістологічних зрізах плаценти методами полімеразної ланцюгової реакції і ДНК–гібридизації.
Етіологія: інфекційна.
Диференційний діагноз:
Фетальний ЦМВ–синдром викликається цитомегаловірусом (ЦМВ), ДНК–вмісним, найбільшим з сімейства герпес-вірусів, в яке входить також вірус простого герпесу, вірус Епштейна–Барр, вірус вітряної віспи – оперізуючого лишая. Людський ЦМВ специфічний для людей і поширений в усьому світі. Більшість випадків інфекції перебігає в субклінічній формі, але якщо у вагітної жінки розвивається первинна інфекція або відбувається реактивізація попередньої інфекції, то вона може передати вірус своєму плоду.
Важливою властивістю всякого герпес-вірусу є те, що, потрапивши в організм, він може реактивовуватись, періодично виділяючись впродовж всього життя господаря. Як первинна, так і рецидивуюча ЦМВ–інфекція можуть супроводжуватись виділенням вірусу, що знаходиться в таких рідинах організму, як слина, сеча, фекалії, кров, сім’яна рідина, цервікальні виділення, грудне молоко. Після первинної ЦМВ–інфекції вірус може виділятись впродовж тривалого часу, і у випадках вродженої, перинатальної чи ранньої постнатальної інфекції він може персистувати впродовж місяців і років. Всі відомі в теперішній час штами ЦМВ – генетично гомологічні, але тільки ті з них, котрі були виділені від хворих, епідеміологічно пов’язаних між собою, характеризуються генетичною ідентичністю.
Передача інфекції:
Хоча ЦМВ – широко розповсюджений збудник і більшість людей заражаються ним на будь-якому етапі свого життя, даний вірус не відрізняється високою контагіозністю. Для його передачі необхідний близький чи інтимний контакт між людьми з інфікованими секретами. Випадковий контакт, вірогідно, не пов’язаний з ризиком зараження. Догляд і звичайні сімейні контакти, котрі можуть супроводжуватись переносом слини чи інших біологічних рідин від людини до людини (як це буває, наприклад, при догляді за маленькою дитиною) також можуть призводити до передачі інфекції. Достовірно встановлена можливість передачі інфекції статевим шляхом. Крім того зараження може відбуватись при переливанні серопозитивної крові чи при трансплантації органів від серопозитивного донора.
ЦМВ–інфекція – найбільш розповсюджена серед виявлених на даний час вроджених інфекцій і добре відома як причина вроджених дефектів. Часто спостерігається також перинатальне інфікування, яке може відбуватись під час пологів, при контакті з кров’ю чи цервікальними виділеннями матері, які містять вірус, або в перші місяці після пологів, якщо серопозитивна мати годує грудьми свою дитину.
Частота:
Повікова частота розвитку ЦМВ–інфекції варіює в різних популяціях в залежності від географічних, етнічних і соціально–економічних факторів.
В країнах, що розвиваються, зараження ЦМВ–інфекцією відбувається в ранньому дитячому віці і більшість молодих дорослих людей серопозитивні. В розвинутих країнах світу, незважаючи на те, що інфекція в дитячому віці зустрічається досить часто, багатьом людям вдається запобігти їй до цілком дорослого віку, і більш важливу роль відіграє передача статевим шляхом. В індивідів з імуносупресією (хворих на СНІД, тих, що проходять курс протиракової терапії, з пересадженим кістковим мозком, трансплантованими органами і т.д.), у малюків раннього віку, чия імунна система недорозвинута, не тільки первинна інфекція, а й реактивація латентної інфекції чи реінфекція новим штамом ЦМВ можуть призводити до найтяжчих форм перебігу. Середній показник на 1000 новонароджених складає близько 3 (від 0,3 до 3% від загальної кількості живонароджених).
Патогенез:
Існує 5 основних шляхів проникнення інфекції в організм вагітної: висхідний, низхідний, гематогенний, трансдецидуальний і змішаний. Після потрапляння вірусу в організм плода формується відповідна імунна відповідь з утворенням антитіл. Подальший прояв інфекції у плода залежить від терміну гестації: генералізована відповідь в ранні терміни, більш локалізована – в більш пізні терміни вагітності. Вірусна ж ДНК знаходиться внутрішньоядерно і при сприятливих умовах (імунодепресивні стани і ін.) відбувається активація інфекції.
Вік прояву:
Клінічні прояви внутрішньоутробних інфекцій залежать від наступних факторів: виду і вірулентності збудника, шляхів проникнення інфекції в організм вагітної, імунологічної реактивності жінки та терміну гестації при інфікуванні.
При внутрішньоутробному інфікуванні на ранніх термінах вагітності формуються інфекційні ембріопатії, котрі проявляються вродженими вадами розвитку, первинною плацентарною недостатністю, що нерідко закінчується самовільним викиднем, завмерлою вагітністю.
Інфікування в більш пізні терміни супроводжується затримкою внутрішньоутробного розвитку плода, формуванням вторинної плацентарної недостатності (часто на фоні плацентиту), локальними і генералізованими ураженнями плода.
Генералізовані форми внутрішньоутробної інфекції частіше розвиваються в ранньому фетальному періоді (І триместр вагітності), так як плід ще не здатний локалізувати запальний процес. В пізній фетальний період (ІІІ триместр) запальні зміни проліферативного характеру викликають звуження чи обтурацію каналів і отворів, що призводить до аномального розвитку вже сформованого органа (гідроцефалія, гідронефроз).
При інфікуванні плода незадовго до народження прояв внутрішньоутробної інфекції залежить від стадії хвороби. Якщо на час пологів захворювання знаходиться в початковій фазі, то інфекція маніфестує в перші три доби раннього неонатального періоду. Якщо пологи припадають на кінцеву стадію хвороби, частіше спостерігається синдром дезадаптації в ранньому неонатальному періоді, в подальшому можлива хронізація процесу, персистуюча латентна інфекція.
Показано, що менше 10% малюків з вродженою інфекцією мають симптоми в неонатальному періоді, але цілком вірогідно, що в подальшому у них виникнуть серйозні ускладнення, до яких відносяться:
- Нейросенсорна глухота;
- Церебральний параліч;
- Епілепсія;
- Затримка психічного розвитку;
- Хоріоретиніт;
- Атрофія зорового нерва;
- Затримка психомоторного розвитку;
- Затримка в розвитку мовлення;
- Нездатність до навчання.
Історія хвороби. Прогноз:
Серед захворювань вагітної, які призводять до інфікування плода і новонародженого, найбільшої уваги заслуговують урогенітальні інфекції (кольпіт, цервіцит, цистіт, безсимптомна бактеріурія, хронічний і гестаційний пієлонефрит), а також хронічні неспецифічні захворювання легень (хронічний бронхіт, бронхіальна астма). До факторів ризику можуть бути віднесені наявність джерел хронічної інфекції в організмі жінки і їх загострення під час вагітності, ускладнений акушерсько–гінекологічний анамнез (хронічний ендометрит, сальпінгоофорит, ерозія шийки матки).
Зважаючи на те, що існує 5 основних шляхів проникнення інфекції в організм вагітної: висхідний, низхідний, гематогенний, трансдецидуальний, змішаний, слід відзначити, що найбільший ризик має висхідний шлях інфікування.
При веденні вагітної звертає на себе увагу низка клінічних ознак: загроза переривання вагітності, затримка розвитку плода, багатовіддя, кольпіт. При інфікуванні в ранньому терміні вагітності можливі ембріопатії, які проявляються вродженими вадами розвитку. Пренатальний діагноз можна встановити, врахувавши клінічні дані пренатальної УЗ–діагностики в поєднанні з лабораторними даними. Пологи проходять per vias naturalis, частіше – передчасні. Кесарів розтин проводити в інтересах плода рекомендують, зваживши позитивні та негативні наслідки, супутню патологію родільні і плода.
При народженні звертає на себе увагу затримка фізичного розвитку, інколи вади (гідро-, мікроцефалія, гідронефроз), гепатоспленомегалія, тромбоцитопенія, петехії, пневмоніт, тривала жовтяниця новонароджених.
У подальшому захворювання може проявитись затримкою психічного розвитку, нервовими порушеннями (церебральний параліч, нейросенсорна глухота, атрофія зорового нерва і т.д.). Не виключається можливість більшої кількості онкохворих з латентною ЦМВ–інфекцією, порівняно з неінфікованими членами популяції. Як правило, фертильність не порушена, хоча частіше може бути невиношування вагітностей.
Лікування:
В даний час не існує рекомендованих методів лікування жінок з діагностованою первинною ЦМВ–інфекцією чи рецидивуючою інфекцією в період вагітності.
Якщо впродовж перших двох триместрів вагітності виявлена первинна інфекція, може виникнути питання про переривання вагітності. ЦМВ–інфекція відрізняється від краснухи тим, що не має жодної стадії вагітності, поза якою ЦМВ не несе особливого ризику; пошкодження, викликані інфекцією, можуть виникнути протягом всіх трьох триместрів. Вірогідність народження малюка з ураженнями, викликаними ЦМВ, у жінок з первинною інфекцією при вагітності складає приблизно 1:25, ще приблизно в половині таких випадків ці ураження швидше за все обмежуються одно– чи двобічним зниження слуху. Якщо інфекція підтверджена при обстежені проби плода, отриманої при амніоцентезі, вірогідність уражень збільшується до приблизно 1:10. Однак, якщо вірус не виділений з амніотичної рідини чи якщо IgM–антитіла не виявлені в пробах крові плода, то це не обов’язково означає, що плід не інфікований.
Поки що не існує безпечного і ефективного методу лікування вродженої чи перинатальної ЦМВ–інфекції з симптомами уражень. Показано, що ацикловір та ганцикловір має первинний ефект при лікуванні ретинохоріоїдиту у хворих з імунодепресією, але ганцикловір високотоксичний. Пропонується фоскарнет, який є інгібітором полімеру ЦМВ та інших герпес-вірусів, нефротоксичний. Рекомендується також загальнозміцнююча терапія та нетрадиційні методи лікування. Проводиться робота по створенню ефективної вакцини.
Профілактика:
Малюки з вродженою чи постнатальною інфекцією можуть виділяти вірус в середовище з сечею, слиною та іншими рідинами організму. Випадкові контакти, найвірогідніше, не призводять до передачі інфекції, через це ізоляція таких малюків недоцільна.
До основних засобів профілактики слід віднести особисту гігієну обслуговуючого персоналу, запобігання гемотрансфузій серопозитивної крові в палатах інтенсивної терапії, з обережністю використовувати донорське молоко. Антенатальний скрінінг на ЦМВ–інфекцію недоцільний, що пов’язано з відсутністю вакцин для серопозитивних жінок. Рекомендацій щодо терміну зачаття після перенесеної первинної ЦМВ–інфекції на даний час не існує. Користування презервативом не гарантує захисту від ЦМВ–інфекції, так як вона може передаватись через слину та інші рідини організму.
Санітарна освіта:
Цю роботу слід зосередити на роз’ясненні механізмів передачі ЦМВ–інфекції і ризиків, пов’язаних з нею, при вагітності.
В стаціонарах необхідно дотримуватись суворого гігієнічного режиму, який включатиме обов’язкове миття рук співробітниками після кожної зміни пелюшок і створення для цього необхідних умов.
Слід регулярно очищувати поверхні та іграшки, які можуть бути контаміновані слиною і сечею.
Література:
- Вродженные, перинатальные и неонатальные инфекции /Под ред. А. Гриноу, Дж. Осборна, Ш. Сазерледн.- Пер. с англ.- М.: Медицина, 2000.- . 59-74.
- Козлова С.И., Демикова Н.С., Семанова Е., Блинникова О.Е. Наследственные синдромы и медико–генетическое консультирование.- М.: Практика, 1996.- C. 275.
- Сидорова И.С., Черненко И.Н. Внутриутробные инфекции: хламидиоз, микоплазмоз, герпес, цитомегалия //ПАГ.- 1999.- № 2.- C. 135-139.
- Сидорова И.С., Черненко И.Н., Сидоров А.А. Особенности лечения и ведения беременности при внутриутробном инфицировании плода //ПАГ.- 2001.- № 1.- C. 27-32.
Переглянуто редакційною колегією I.B.I.S.: 11/11/2002
Дивіться також:
- Цитомегаловірусна інфекція (інформація для батьків)
Цитомегаловірусна інфекція
(Congenital Cytomegalovirus (CMV) Infection)
О.О. Михасюк
Спеціаліст з інформаційного забезпечення
Українсько-Американської Програми запобігання вродженим вадам розвитку
Протягом останніх років відмічається тенденція до збільшення серед вагітних жінок частоти вірусних інфекцій та зростання їх здатності до епідемічного поширення. При цьому особливого значення набуває цитомегаловірусна інфекція (ЦМВІ), яка може спричиняти виникнення акушерської патології, ембріо- та фетопатій, внутрішньоутробних та перинатальних інфекцій.
Наявність латентних форм ЦМВІ з атиповим перебігом, інаппарантним проявом та ураженням тканин органів становить серйозну проблему для своєчасного розпізнавання інфекції та є причиною діагностичних помилок.
Серед живонароджених 0,2-2,2% дітей мають внутрішньоутробне інфікування цитомегаловірусом. Внутрішньоутробна ЦМВІ, незалежно від форми захворювання, може уражати центральну нервову систему та призводити до виникнення психомоторних порушень, розумової відсталості дітей, навіть через кілька років після народження.
В епідеміології ЦМВІ відсоток вагітних жінок є надзвичайно високим. Цитомегаловірусна інфекція виявляється в них в два рази частіше, ніж краснуха.
ЦМВІ може викликати розвиток ускладнень під час вагітності, пологів та в післяпологовому періоді. Акушерська патологія найчастіше проявляється у вигляді спонтанних абортів, мертвонароджень або народження дітей, нездатних до життя.
Механізм зараження цитомегаловірусною інфекцією:
Цитомегаловірус належить до родини герпетичних вірусів. Відомо близько 40 їх різновидів. Для людини патологічними є вісім герпетичних вірусів: звичайний герпес (І та ІІ типів), цитомегаловірус, вірус вітряної віспи (оперізуючого лишаю), вірус Епштейна-Барра, а також вірус герпесу VI, VII та VIII типів. Вони викликають загострення хронічної інфекції та демонструють здатність до персистування в організмі.
Цитомегаловірус є крупним ДНК–вірусом з порівняно невисокою вірулентністю та особливою здатністю до різкого пригнічення клітинного імунітету.
Джерелами інфекції можуть бути носії ЦМВ, їх біологічні рідини та виділення: кров, сеча, сльози, слина, грудне молоко, спинномозкова або амінотична рідина, слиз, сперма тощо. Але найпоширенішим агентом передачі ЦМВІ є слина. Тому переважна кількість заражень припадає на такі пари, як мати–дитина та статеві партнери. З урахуванням віку та інтимності контактів між людьми виявляють дві хвилі захворюваності на ЦМВІ: перша припадає на вік від народження до 3 років, друга – на період статевого дозрівання.
В переважній більшості випадків спостерігається безсимптомне вірусоносійство або хронічна інфекція, що не викликає ніяких порушень і не має клінічних проявів. Але при активному перебігу хвороби цитомегалічні зміни в першу чергу спостерігаються в слинних залозах, легенях, нирках та головному мозку.
ЦМВІ та вагітність:
Питання про вплив терміну вагітності на передачу інфекції від матері до плоду залишається відкритим. Переважна більшість науковців схиляється до думки, що найбільшу загрозу для плода становить розвиток ЦМВІ в першій половині вагітності. Є кілька шляхів передачі інфекції від матері до плоду:
- Трансплацентарний.
- Через інфіковані виділення в родовому каналі.
- Годування інфікованим материнським молоком.
Найчастіше до інфікування плоду призводить трансплацентарна передача ЦМВІ. Цитомегаловірус від матері може проникати через плаценту в будь-якому терміні вагітності та викликати ураження плоду. ЦМВІ у вагітних може бути первинною та вторинною. Вроджена ЦМВІ виникає або після первинної інфекції, або в результаті загострення хронічної. Більш важкі наслідки для дитини спостерігаються при первинній інфекції у матері в період вагітності.
Механізм передачі ЦМВІ через плаценту передбачає тісний контакт між вагітною (породіллею) та плодом (новонародженим). Після вагітності та пологів ЦМВІ можна знайти майже в усіх рідинах тіла, особливо в цервіко-вагінальних виділеннях і в грудному молоці, що може стати джерелом пери- та постнатальної передачі ЦМВІ від матері до новонародженого.
Передача інфекції може відбутися з кров’ю під час переливання та при парентеральних маніпуляціях, а також через пошкоджену шкіру та ушкоджені слизові оболонки. Достеменно відомо, що інтранатальна або рання постнатальна передача ЦМВІ відбувається в 10 (!) разів частіше, ніж трансплацентарна.
Перинатальні та постнатальні прояви ЦМВІ у дітей майже завжди мають легкий та асимптоматичний перебіг. Варіанти перебігу ЦМВІ у вагітних та дітей пов’язані зі складністю взаємовідношень між ЦМВ та клітиною господаря. Часто клінічні симптоми проявляються у вигляді субфебрильної температури, ринофарингіту або кашлю. Для вагітних більш притаманна форма ЦМВІ, яка, зазвичай, не має клінічних проявів. Проте у даної категорії жінок в анамнезі часто зустрічається звичне невиношування вагітності або вагітність, що не розвивається, мертвонародження, народження нежиттєздатних дітей та дітей з вродженими вадами розвитку.
Як вже зазначалося вище, інфікування можливе в будь-якому терміні вагітності, але найважчі наслідки виникають при первинному інфікуванні, що відбувається впродовж перших 20 тижнів вагітності. Внутрішньоутробне інфікування ЦМВ може призвести до народження дітей з важкими неврологічними порушеннями, ураженням зорового та слухового нервів. Ступінь ураження плоду залежить від терміну інфікування. Зараження в ранньому терміні вагітності найчастіше призводить до загибелі плоду та спонтанних абортів. Діти з ЦМВІ мають меншу вагу та зріст при народженні, ніж здорові. ЦМВ може інфікувати плаценту, плід, амніотичну рідину. Разом із тим, навіть за умови розвитку первинної ЦМВІ під час вагітності, 90-95% жінок мають шанс народити здорову дитину.
Вроджена форма ЦМВІ, як правило, характеризується генералізованим ураженням органів плода і цілим комплексом клінічних симптомів. Для набутої форми ЦМВІ притаманний латентний перебіг, переважно з локальним ураженням слинних залоз. У новонароджених, які зазнали внутрішньоутробного інфікування, в 90% випадків не буває симптомів при народженні, у 5-7% з них розвиваються ускладнення в пізнішому періоді. Розвиток симптоматики в новонародженої дитини корелює з симптомами, що були наявні на момент народження.
Клінічні форми ЦМВІ:
Клінічні форми ЦМВІ можуть мати гострий або хронічний перебіг. Відповідно до ступеня важкості проявів ЦМВІ виділяють:
- легку форму (в тому числі стерті та субклінічні форми інфекції), при якій ураження внутрішніх органів є незначним та не супроводжується функціональними порушеннями (компенсація);
- середньої важкості, при якій відбувається ураження внутрішніх органів, яке супроводжується функціональними порушеннями різного ступеня (субкомпенсація);
- важку форму, при якій спостерігається різко виражена інтоксикація та ураження внутрішніх органів з важкими функціональними порушеннями (декомпенсація).
Легка форма зазвичай асоціюється з гострим респіраторним захворюванням. При цьому хворі скаржаться на слабкість, швидку втому, болі голови, нежить, тощо. При легкій формі хвороба набуває хвилеподібного характеру. Середня форма супроводжується множинним ураженням внутрішніх органів (запалення печінкової тканини, наднирників, селезінки, підшлункової залози, нирок). Також частими є безпричинні пневмонії, зниження рівня тромбоцитів в крові, ураження судин очей, стінок кишечника, головного мозку та периферичних нервів. При важкій формі ЦМВІ смерть дитини найчастіше наступає в перші дні або тижні життя. В дорослих жінок важка форма ЦМВІ провокує розвиток запалення та ерозії шийки матки, внутрішнього шару матки, піхви та яйників.
Слід відмітити, що діти з вродженою або перинатальною активною цитомегалією мають надзвичайну схильність до розвитку бактеріальних субінфекцій, що обумовлено в першу чергу імунною недостатністю.
Симптоми вродженої ЦМВІ включають ознаки затримки внутрішньоутробного розвитку, внутрішньоутробну гіпотрофію, кон’югаційну жовтяницю, гепатоспленомегалію, порушення мозкового кровообігу, тощо. Частими є ускладнення з боку ЦНС – підвищена сонливість, поганий смоктальний рефлекс, макро- та мікроцефалія, гідроцефалія, поренцефалія, сенсоневральна глухота тощо.
Вроджена ЦМВІ може мати незвичні прояви, такі, як вентрикуломегалія, перивентрикуліт або утворення кіст, гемолітична анемія, хронічний гепатит, асцит тощо.
Незважаючи на велику кількість симптомів та ускладнень, що асоціюються з вродженою ЦМВІ, одразу після народження важко передбачити, яким буде фізичний та інтелектуальний розвиток дитини.
Ускладнення ЦМВІ:
Гепатомегалія разом із спленомегалією є найбільш переконливим доказом хвороби у дитини з вродженою ЦМВІ. Зазвичай є присутніми явища гепатиту з порушенням функції печінки (жовтуха, гіпербілірубінемія), які, як правило, нормалізуються в перші тижні життя. Спленомегалія часто може бути єдиним показником вродженої ЦМВІ при народженні.
При дослідженнях крові виявляється картина гіпохромної анемії, еритробластоз, тромбоцитопенія.
Вроджена ЦМВІ призводить до порушення зору в 20% дітей. Найчастіше спостерігається хоріоретиніт (одно- чи двобічний), який може призвести до сліпоти. Але ЦМВІ зазвичай не викликає катаракти або мікрофтальмії.
Мікроцефалія може частково спричиняти затримку розвитку новонародженого та поєднуватись з внутрішньочерепними кальцифікатами, які локалізуються в перивентрикулярній структурі та лікворі. Комп’ютерна томографія є найчутливішим методом діагностики. Ультразвук та рентгенографія черепа відносяться до менш чутливих методів. Більшість дітей з мікроцефалією та внутрішньочерепними кальцифікатами мають неврологічні порушення.
У 10% дітей з асимптоматичними проявами інфекції можуть спостерігатися ускладнення, навіть у віці 5-7 років, найчастіше у вигляді сенсорної втрати слуху, неврологічних розладів або розумової відсталості. Половина дітей з вродженою ЦМВІ мають комбіновану втрату слуху. Глухота носить двобічний сенсоневральний характер. Нерідко також діагностуються вроджені серцево-судинні, шлунково-кишкові, м’язево-скелетні аномалії розвитку.
Таким чином, для вагітних з цитомегаловірусною інфекцією має передбачатися комплекс діагностичних, профілактичних та лікувальних заходів, скерованих на зниження кількості випадків виникнення вродженої цитомегаловірусної інфекції, що має бути обов’язковою умовою створення ефективної системи профілактики та охорони здоров’я матері та дитини.
Лікування ЦМВІ:
Лікування цитомегаловірусної інфекції є досить складним. На сьогоднішній день є не так багато препаратів, які були б ефективними по відношенню до даного вірусу. Але при вродженій або перинатальній формі ЦМВІ специфічного лікування не існує.
Більшість вчених вважає, що повністю вилікувати ЦМВІ неможливо. Також, неможливим є видалення цитомегаловірусу з організму. Проте, у випадках ранньої діагностики та відповідного лікування є шанс протягом тривалого часу утримувати хворобу в “сплячому” стані. Це надзвичайно важливо для забезпечення нормального виношування вагітності та народження здорової дитини.
Переглянуто редакційною колегією I.B.I.S.: 12/06/2002
Дивіться також:
Ізотретіноїновий (вітамін А) синдром
(Accutane (Isotretinoin) Syndrome)
Т.В. Віговська
Зав. неонатологічним центром
Волинського обласного дитячого територіального медичного об’єднання
Ізотретіноїн (аккутан, рокутан) застосовується для лікування акне. Це 13-цис-ретінова кислота, один із вітамін А-подібних засобів, описаних як ретіноїди. Незважаючи на те, що здатність вітаміну А викликати вроджені вади у тварин відома понад 30 років, зростаюче використання його похідних у лікуванні вугрів та псоріазу викликає пильну увагу.
Клінічні прояви:
Серед аномалій, що їх викликає вітамін А – симптоми подібні до синдрому Ді Джорджі : краніофаціальні аномалії асоціюються с серйозними вадами розвитку центральної нервової системи типу гідроцефалії чи кист мозку. Зустрічається кортікальна сліпота та параліч лицьового нерва. Дисморфічні риси обличчя також включають асиметрію лиця з мідфаціальною гіпоплазією, мікрофтальмію, окорухові порушення, розщелину піднебіння та губи, мікротію та аномалії зовнішнього слухового ходу.
Найбільш характерні дефекти інших органів та систем включають серцево-судинні аномалії, такі як гіпоплазія дуги аорти, ДМШП, транспозицію магістральних судин, гіпоплазію лівого шлуночка.
Серед описаних дефектів називають: дефекти невральної трубки, трахеостравохідну норицю, гіпоплазію наднирників, гіпоплазію стегнової кістки, клишоногість, синдактилію.
Диференціальний діагноз:
- синдром Ді-Джорджі
- синдром Бікслера
- окуло-аурикуло-вертебральна дисплазія
Профілактика:
Враховуючи, що період піврозпаду ізотретіноїну приблизно 50 годин, слід припинити його використання принаймі за 10 днів до можливого зачаття.
Застереження:
Надійна контрацепція повинна проводитись щонайменше за 1 місяць до початку терапії ізотретіноїном, під час лікування і 1 місяць після припинення його використання за виключенням пацієнток після гістероектомії та тих, що знаходяться в періоді менопаузи більше 1 року. Слід використовувати 2 надійних методи контрацепції одночасно. Ще до початку терапії у жінок дітородного віку (за 24 години до прийому першої таблетки) слід провести тест на вагітність і повторювати цей тест щотижня, поки триває лікування. Якщо вагітність все ж наступила, прийом ізотретіноїну слід негайно припинити. Щодо чоловіків, то, приймаючи ізотретіноїн і маючи статеві стосунки з жінками дітородного віку, вони обов’язково повинні використовувати бар’єрні контрацептиви.
Список літератури:
- Cordero J, Kochhar D, Fantel A. Recommendations for isotretinoin use in women of childbearing potential. Teratology 1991;44:1-6.
- Fantel FG, et al. Teratogenic effects of retinoic acid in pigtail monkeys (Macaca Nemestrina). Teratology 1977;15:65-71.
- Gorlin RJ, Cohen MM, Levin LS. Vitamin A congeners. In: Syndromes of the Head and Neck. 3d ed. Oxford: Oxford University Press, 1990:20-21.
- Lammer EJ, et al. Retinoic acid embryopathy. New England Journal of Medicine 1985;313:837-841.
- Pastuszak A, Koren G, Rieder MJ. Use of Retinoid Pregnancy Prevention Program in Canada: Patterns of contraception use in women treated with isotretinoin and etretinate. Reproductive Toxicology 1966;8(1):63-68.
Переглянуто редакційною колегією I.B.I.S.: 02/07/2000
Дивіться також:
- Аккутан та інші ретиноїди (інформація для батьків)
Культура та ціна. Вплив ідей
“Допомога дітям з вродженими вадами розвитку чи спадковими захворюваннями, застосування у їх лікуванні дорогих хірургічних та медичних засобів іноді викликає критику … Інколи кажуть, що занадто багато робиться для скалічених і розумово відсталих … Здається, сьогодні немає необхідності жертвувати слабким заради сильного … Наше суспільство і наші закони захищають і гарантують людське життя, досконале воно чи недосконале … Були й інші суспільства … Милосердне ставлення до слабкого, скаліченого і розумово відсталого може здаватися ірраціональним для розумного аналітика, але, очевидно, воно має благотворний вплив на саме суспільство, виховує його … Діти з вадами багато чому вчать нас, … і багато чому ми навчаємось у процесі їх лікування і навчання … Це ціна, яку повинні заплатити ті, хто має нормальних дітей, ціна за подолання варварства і жорстокості, що притаманні тим суспільствам, які знищують слабких і скалічених.”
(Із вступу до розділу “Сучасні тенденції в тератології” в книзі Дж. Варкані “Вроджені вади розвитку”.- Year Book Publ., 1971.- с.28).
“Расова гігієна” – батько і син
Лікарі фон Фріц Ленц (1887-1970) і його син, фон Відукінд Ленц (1919-1995), стали добре відомими німецькими медичними генетиками. Дехто вважає, що батько мав скоріше ганебну репутацію. Проте, мало хто зможе поставити під сумнів заслужену славу доктора фон Відукінда Ленца, вклад якого добре описаний в статті його співвітчизників Дж. М. Опітца і Г.Р. Відеманна (Am. J. Med. Genet.- 1996.- т.65.- с.142).
Вчені все ще сперечаються, чи брав участь доктор фон Фріц Ленц у політиці “расової гігієни” в нацистській Німеччині (Р.Н. Проктор “Расова гігієна”.- Кембрідж: Harvard Univ. Press, 1988). “Раса – основна цінність”,- цього догмату фон Ф. Ленц дотримувався усе життя. Через рік після закінчення другої світової війни фон Ф. Ленц зміг відновити свій статус професора генетики, у той час як його син Відукінд все ще був військовополоненим.
Внесок доктора фон Відукінда Ленца є більш позитивним і підтверджує його міжнародне визнання. Доктор Г.Р. Відеманн писав, що доктор Шафер, тоді головний педіатр, “… всіляко заохочував Ленцові дослідження причин епідемії вроджених вад розвитку в 1961 році (Am. J. Med. Genet.- 1996.- т.65.- с.143).
Після подій 1962 року, пов’язаних із талідомідом, Відукінд Ленц зробив багато для усвідомлення причин виникнення вроджених вад розвитку та розуміння ролі генетики.