Serhiy
Подвійне відходження магістральних судин від правого шлуночка
(Double Vessel Outlet)
Н.О. Лобінцева
Лікар УЗД
Хмельницької міської дитячої лікарні
Діагноз:
Подвійне відходження магістральних судин від правого шлуночка (ПВМС) – це комбінована вроджена вада серця (ВВС), при якій легеневий стовбур і аорта відходять від правого шлуночка. Вперше описано у 1866 році Paecock.
Діагностичні критерії:
Основні ознаки подвійного відходження магістральних судин з правого шлуночка:
- Головна ознака – переважне відходження обох судин – аорти і легеневої артерії від правого шлуночка серця.
- Два вихідні відділи в правому шлуночку – для аорти і легеневої артерії.
- Відсутність мітрально-аортального продовження.
- Наявність дефекту міжшлуночкової перегородки – єдиний шлях для опорожнення лівого шлуночка.
Вирізняють наступні варіанти ПВМС:
- Класичний варіант – відходження аорти і легеневої артерії від правого шлуночка з обов’язковим порушенням мітрально-аортального продовження.
- Синдром Тауссіг-Бінга – відходження аорти і легеневої артерії від правого шлуночка з підлегеневим розташуванням дефекту міжшлуночкової перегородки (ДМШП) з обов’язковим порушенням мітрально-аортального продовження.
- Відходження аорти і легеневої артерії від правого шлуночка з дефектом міжшлуночкової перегородки в стороні від устя аорти і легеневої артерії.
- Подвійне відходження магістральних судин з анатомією, характерною для тетради Фалло.
- Подвійне відходження магістральних судин від правого шлуночка з дефектом міжшлуночкової перегородки, який розташований над надшлуночковим гребнем.
Гемодинамічні порушення залежать від:
- розмірів і розташування ДМШП, який може бути:
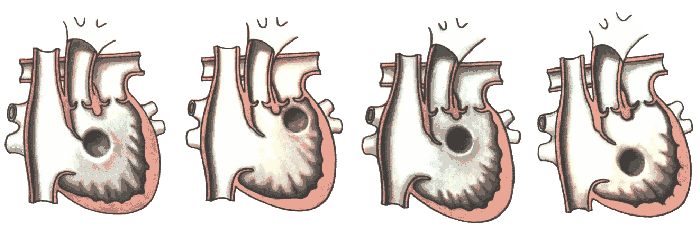
- підаортальним (рисунок крайній зліва );
- підлегеневим (рисунок другий зліва);
- під обома магістральними судинами (рисунок третій зліва);
- віддалений від обох магістральних судин (рисунок крайній справа).
- наявності чи відсутності стенозу легеневої артерії;
- стану трьохстулкового клапану і прикріплення хордального апарату і сосочкових м’язів.
При підаортальному розташуванні ДМШП – венозна кров із правого шлуночка одним потоком поступає в легеневу артерію, а артеріальна кров через дефект міжшлуночкової перегородки в аорту. В цьому випадку у хворих артеріальна гіпоксемія відсутня або дуже незначна, тому що в велике коло кровообігу поступає в основному артеріальна кров. З народження визначається гіперволемія малого кола кровообігу. Ціанозу немає, але рано з’являється легенева гіпертензія. Якщо при такому розташуванні ДМШП є стеноз легеневої артерії, то гіпоксемія виражена з моменту народження.
При підлегеневому розташуванні ДМШП – в легеневу артерію поступає переважно артеріальна кров із лівого шлуночка, а в аорту – змішана венозна кров із правого шлуночка. Тому у цих хворих поряд із гіперволемією малого кола кровообігу виявляють значну артеріальну гіпоксемію і рано розвивається висока легенева гіпертензія.
Клінічні прояви вади:
Клінічно всі форми вади протікають важко, із швидким розвитком тяжких порушень гемодинаміки, легеневою гіпертензією і артеріальною гіпоксемією.
При спонтанному закритті ДМШП – наступає раптова смерть.
При підаортальному розташуванні ДМШП – клінічні прояви схожі із ізольованим ДМШП із високою легеневою гіпертензією. Швидко розвивається гіпотрофія ІІ-ІІІ ст., характерні рецидивуючі пневмонії, серцева недостатність, яка рефрактерна до лікування. Ціаноз з’являється при крику, що свідчить про вено-артерільне шунтування, у старших дітей є ознакою високої легеневої гіпертензії. Характерна задишка по типу тахіпное з участю допоміжної мускулатури. Аускультативно – вислуховується пов’язаний із І тоном грубий систолічний шум зліва на рівні 2-4 міжребер’я. Над легеневою артерією визначається акцентований, розщеплений ІІ тон; тут же при легеневій гіпертензії можуть вислуховуватися кліки, короткий протодіастолічний шум.
При наявності стенозу легеневої артерії клінічна картина абсолютно схожа з тетрадою Фалло. Характерні: задишка, грубий сістолічний шум запаморочення, ціаноз, а також задишечно-ціанотичні напади, які починаються раптово, дитина стає стурбована, посилюється задишка, ціаноз, зменшується інтенсивність шуму, потім можливе апное, втрата свідомості (гіпоксична кома).
При аномалії Тауссіг-Бінга (з підлегеневим розташуванням ДМШП) клінічна картина аналогічна повній транспозиції магістральних судин. З народження спостерігається генералізований ціаноз, задишка, відставання в фізичному розвитку. Вислуховується грубий систолічний шум з епіцентром в четвертому міжребер’ї біля правого краю грудини і виражений акцент ІІ тона над основою серця. Швидко розвивається гіпоксемія і серцева недостатність, після 1-3 місяців життя з’являється гіпотрофія, яка пов’язана з труднощами годування, відставання в моторному розвитку. Гіпоксемічні напади виникають не часто.
Поєднані симптоми:
У 60% випадків ПВМС із правого шлуночка поєднується із іншими ВВС:
- дефект міжшлуночкової перетинки (ДМШП) – вада, яка необхідна для життя;
- стеноз легеневої артерії – найчастіше поєднується із ПВМС із правого шлуночка і впливає на гемодинаміку та клінічні прояви;
- коарктація аорти;
- аномалія правої коронарної артерії;
- відкрита артеріальна протока;
- дефект міжпередсердної перетинки (ДМПП).
У 12,5% випадків ваду може супроводжувати екстракардіальна патологія:
- відсутність селезінки;
- аномалія положення органів;
- трахеостравохідна фістула;
- щілина твердого піднебіння і верхньої губи.
ПВМС із правого шлуночка може входити до складу:
- геніто-палато-кардіального синдрому Гартнера-Силенго-Ваштеля (ОМІМ 231060) – включає також гіпоспадію, розщеплення твердого та м’якого піднебіння, мікрогнатію;
- синдрому конотрункальних аномалій (ОМІМ 217095) – транспозиція магістральних судин, спільний артеріальний стовбур, мікроделеція 22q 11.2;
- синдрому летальних мальформацій Бімера (ОМІМ 209970) – гідроцефалія, гермафродитизм, тромбоцитопенія, специфічне обличчя з бульбоподібним носом і широким переніссям, витончені кістки;
- Трисомії 13 (синдром Патау) – мікроцефалія, щілина губи і піднебіння, полідактилія, мікрофтальмія, лицьові дизморфії, множинні вади розвитку внутрішніх органів.
Дані обстежень:
ЕКГ:
- при підаортальному розташуванні ДМШП без стенозу легеневої артерії – ознаки комбінованої гіпертрофії шлуночків серця з відхиленням електричної вісі серця;
- при підаортальному розташуванні ДМШП із стенозом легеневої артерії – відхилення електричної вісі вправо, порушення атріо-вентрикулярної та внутрішньошлуночкової провідності;
- при підлегеневому розташуванні ДМШП (аномалія Тауссіг-Бінга) – відхилення електричної вісі серця вправо, ознаки гіпертрофії правого передсердя і шлуночка.
ФКГ: дані не специфічні. Виявляють ознаки легеневої гіпертензії, стенозу легеневої артерії.
Рентгенологічна картина – неспецифічна. При стенозі легеневої артерії рентгенологічні ознаки нагадують картину при тетраді Фалло: незначне збільшення розмірів серця, внаслідок гіпертрофії стінок правого шлуночка і помірного розширення його порожнини, серце нагадує дерев’яний черевичок. Легеневий малюнок виражений нечітко. При аномалії Тауссіг-Бінга поряд з ознаками легеневої гіпертензії відмічається більш виражене вибухання легеневої артерії, ніж у хворих із подвійним відходженням магістральних судин по типу тетради Фалло, але без стенозу легеневої артерії.
Ультразвукова діагностика: цьому методу діагностики належить основна роль серед неінвазивних методів діагностики.
У позиції по довгій вісі лівого шлуночка із парастернального доступу візуалізуються:
- Дві магістральні судини, які відходять від правого шлуночка і мають паралельний хід. Півмісяцеві клапани аорти і легеневої артерії розташовані на одному рівні.
- Мітрально-півмісяцеве фіброзне продовження відсутнє. Візуалізується бульбарно-вентрикулярна складка, яка розділяє мітральний клапан і півмісяцевий клапан судини.
- Деформація вихідного відділу лівого шлуночка у вигляді Z-подібної конфігурації.
- Дефект міжшлуночкової перетинки.
У позиції по короткій вісі аорти із парастернального доступу встановлюють:
- розташування ДМШП;
- наявність стенозу легеневої артерії;
- взаємовідношення аорти і легеневої артерії;
- визначається розходження конусної перегородки, яка розділяє магістральні судини;
- відсутність сформованного надшлуночкового гребеня.
У чотирикамерній позиції із верхівкового та субкостального доступу визначають локалізацію ДМШП.
Доплерографія: допомагає в діагностиці супутніх клапанних змін – стеноз, недостатність, дефектів міжшлуночкової та міжпередсердної перегородок, дає можливість визначити градієнт тиску між лівим та правим шлуночком, аортою та правим шлуночком.
Остаточний діагноз вади може бути поставлений після проведення ангіографії.
Етіологія:
В більшості випадків причина виникнення цієї вади серця, як і інших ВВС, невідома. В 90% випадків вона має поліґенно-мультифакторіальне наслідування.
Патогенез:
Виникнення вади пов’язують з відсутністю процесу резорбції в примітивній сердечній трубці бульбарно-вентрикулярного гребня, що не дозволяє аорті після поділу загального артеріального стовбура переміститися в лівий шлуночок. Гребінь, який представлений міокардіальною тканиною, вклинюється між півмісяцевими та мітральним клапаном, утворюючи внутрішній край дефекту міжшлуночкової перетинки і обумовлюючи відсутність мітрально-півмісяцевого фіброзного продовження. Також при цьому відсутнє і легенево-трикуспідальне продовження. Ця вада виникає на 29-31 день запліднення.
Співвідношення між статтю: Ч 1 : Ж 1.
Частота виникнення:
Це вада серця, яка зустрічається відносно рідко – 1% від усіх ВВС. 1 : 125000.
Диференційний діагноз:
Необхідно проводити з дефектом міжшлуночкової перетинки, відкритим атріовентрикулярним каналом, тетрадою Фалло, повною транспозицією магістральних судин.
Лікування:
Може бути тільки оперативним. Для визначення можливості і характеру оперативного втручання необхідно чітко знати:
- Величину і взаємовідношення ДМШП з магістральними судинами.
- Взаємовідношення аорти і легеневого стовбура.
- Наявність чи відсутність стенозу легеневої артерії.
- Патологію атріо-вентрикулярних клапанів.
- Прикріплення хордального апарату і сосочкових м’язів.
- Ступінь легеневої гіпертензії.
При відсутності стенозу легеневого стовбура і легеневих артерій радикальна корекція вади показана в віці 12-24 міс.
У дітей раннього віку при поєднанні вади із стенозом легеневої артерії показано накладання міжартеріального анастомозу. Радикальна корекція вади при наявності стенозу легеневого стовбура показана у дітей старше 4 років.
При обструктивному ДМШП показане раннє оперативне втручання.
Вперше успішна радикальна коррекція класичного типу подвійного відходження магістральних судин від правого шлуночка була виконана в 1957 р. Kirklin.
Якщо ДМШП розташований в стороні від вустя магістральних судин, то хірургічна корекція вади становить значні труднощі.
Радикальна корекція виконується у хворих у віці старше 5-6 років. До цього віку виконують паліативну операцію – звуження легеневого стовбура або накладання міжартеріального анастомозу.
При аномалії Тауссіг-Бінга корекція вади значно складніша, тому що при цьому варіанті ПВМС від правого шлуночка важко створити пряме сполучення лівого шлуночка і аорти через віддаленність ДМШП від вустя аорти.
Основні причини смерті після хірургічної коррекції:
- гостра серцево-судинна недостатність, яка обумовлена високою легеневою гіпертензією;
- некориговані супутні вади;
- порушення ритму серця;
- високий систолічний градієнт тиску між лівим шлуночком і аортою;
- пошкодження коронарних артерій.
Найкращі віддалені післяопераційні результати спостерігаються при підаортальному розташуванні ДМШП.
Допологова діагностика:
Допологова діагностика затруднена, тому що вада не спричиняє антенатального порушення гемодинаміки. Специфічна пренатальна діагностика подвійного відходження магістральних судин із правого шлуночка викликає труднощі, оскільки ознаки тетради Фалло, транспозиції магістральних судин дуже схожі.
Прогноз:
Визначається варіантом подвійного відходження магістральних судин, наявністю супутніх патологій. Без хірургічного лікування прогноз захворювання несприятливий. Більшість хворих з легеневою гіпертензією гинуть на першому році життя. Тривалість життя більша, коли вада поєднується зі стенозом легеневої артерії і хворі доживали до 25-35 років. Смертність на першому році життя досягає 40%.
Профілактика:
Враховуючи важкість стану після народження, високу летальність після оперативних втручань, у 40% неоперабельність хворих, перевага віддається перериванню вагітності, особливо при поєднанні з іншими вадами розвитку.
Необхідно у всіх випадках виявлення вади проводити ретельне обстеження плоду для виключення поєднаних серцевих та позасерцевих аномалій, у тому числі визначення каріотипу. Рекомендується проводити динамічне ультразвукове обстеження з метою визначення ознак застійної серцевої недостатності. Поєднання водянки плоду із структурними дефектами серця відноситься до загрозливих ознак. Раціональна акушерська тактика не розроблена до кінця. Оптимальним може бути дострокове родорозрішення, але батьки повинні знати, що смертність дітей при цій ваді дуже висока. При відсутності ознак застійної серцевої недостатності стандартна акушерська тактика не має альтернативи, але родорозрішення потрібно проводити в спеціалізованих центрах, де можливе надання необхідної кардіохірургічної допомоги.
Номер з каталогу МІМ:
217095 Conotrunkal Heart Malformation; CHTM
231060 Genitopalatocardiac Syndrome
209970 Beemer Lethal Malformation Syndrome
Література:
- Белозеров Ю.М., Болбиков В.В. Ультразвуковая диагностика и симеотика в кардиологии детского возраста.- М.: Медпресс, 2001.
- Белоконь Н.А., Подзолков В.П. Врожденные пороки сердца.- М.: Медицина, 1991.
- Детская ультразвуковая диагностика /Под общей редакцией М.И. Пыкова, К.В. Ватолина.- М.: Издательский дом Видар-М, 2001.
- Затикян Е.П. Кардиология плода и новорожденного.- М.: Инфо-медиа, 1996.
- Ромеро Роберто. Пренатальная диагностика врожденных пороков развития плода.- М.: Медицина, 1994.
- Сердечно-сосудистая хирургия /Под ред. В.И. Бураковского, Л.А. Бокерия.-М.: Медицина, 1989.
- Brewer S, Jiang X, Donaldson S, Williams T, Sucov HM. Requirement for AP-2alpha in cardiac outflow tract morphogenesis. Mech Dev 2002 Jan;110(1-2):139-49.
- Brown JW, Ruzmetov M, Okada Y, Vijay P, Turrentine MW. Surgical results in patients with double outlet right ventricle: a 20-year experience. Ann Thorac Surg 2001 Nov;72(5):1630-5.
- Fraisse A, Ghez O, Ligi I, Laporte-Giugliano V, Chetaille P, Bonnet JL, Aubert F, Metras D. Dextrocardia with situ solitus, ventricular loop, double outlet hypoplastic right ventricle and L-malposition of the great arteries. Description and surgical treatment of a rare and complex cardiopathy. Arch Mal Coeur Vaiss 2002 May;95(5):495-9.
- Freedom RM, Yoo SJ. Double-outlet right ventricle: Pathology and angiocardiography. Semin Thorac Cardiovasc Surg Pediatr Card Surg Annu 2000;3:3-19.
- Goldmuntz E, Bamford R, Karkera JD, dela Cruz J, Roessler E, Muenke M. CFC1 mutations in patients with transposition of the great arteries and double-outlet right ventricle. Am J Hum Genet 2002 Mar;70(3):776-80.
- Ito M, Takagi N, Sugimoto S, Oosawa H, Abe T. Pregnancy after undergoing the Fontan procedure for a double outlet right ventricle: report of a case. Surg Today 2002;32(1):63-5.
- Lascano ME, Schaad MS, Moodie DS, Murphy D Jr. Difficulty in diagnosing double-chambered right ventricle in adults. Am J Cardiol 2001 Oct 1;88(7):816-9.
- Manner J. On the value of morphogenetic classifications of hearts with double outlet right ventricle. Cardiol Young 2001 Nov;11(6):689-90.
- Oshima Y, Yamaguchi M, Yoshimura N, Oka S, Ootaki Y. Anatomically corrective repair of complete atrioventricular septal defects and major cardiac anomalies. Ann Thorac Surg 2001 Aug;72(2):424-9.
- Puga FJ. The role of the Fontan procedure in the surgical treatment of congenital heart malformations with double-outlet right ventricle. Semin Thorac Cardiovasc Surg Pediatr Card Surg Annu 2000;3:57-62.
- Smallhorn JF. Double-outlet right ventricle: An echocardiographic approach. Semin Thorac Cardiovasc Surg Pediatr Card Surg Annu 2000;3:20-33.
Переглянуто редакційною колегією I.B.I.S.: 02/10/2002
Програма тренувань для волонтерів, залучених до проекту запобігання розумовій відсталості у дітей-сиріт
Кетрін Уоткінс
Волонтер Українського Альянсу із запобігання
вродженим вадам розвитку
К. Уоткінс більше 22 років досліджувала різні аспекти навчання дітей з особливими потребами. За цей час вона працювала академічним директором Паризької спеціальної освітньої школи у Франції, викладала в ліцеї м. Нью-Йорка, навчала підлітків з сильним розумовим відставанням у школі району Санта-Барбара (Каліфорнія), а також заснувала франко-американську школу в м. Нью-Йорку. Діти із спеціальними потребами є пристрастю усього її життя. В цій статті вона щиро ділиться своїм досвідом.
Українсько-Американська Програма запобігання вродженим вадам розвитку (УАПЗВВР) використовує цей навчальний посібник в ході виконання Проекту ранньої стимуляції дітей-сиріт. Цей пілотний проект реалізується в м. Рівному за участю Рівненського центру УАПЗВВР, Рівненського Дитячого Будинку та Рівненського державного гуманітарного університету. В 2002 році перша група студентів-волонтерів університету закінчила тренування і приступила до роботи з малюками.
Вступ
Перед тим, як волонтери розпочнуть будь-яку роботу з дітьми-сиротами, необхідно провести для них спеціальний навчальний курс з питань нормального розвитку дитини та найпоширеніших вроджених вад розвитку (ВВР), з якими вони можуть зіткнутися під час роботи в будинку дитини. Вони повинні розуміти можливості розвитку неповноцінних дітей, прояви їхніх вад та ті спеціальні потреби, що виникають внаслідок ураження. По закінченні курсу волонтери мають знати подану нижче інформацію.
Роль волонтерів полягає в надані відповідної допомоги в емоційному та фізичному розвитку дитини, сприяти розвитку органів чуття й стимулювати розумовий розвиток дитини.
Нижче поданий опис основних етапів розвитку дитини, на яких підтримка дорослих опікунів буде максимально ефективною. Я сподіваюсь, що студенти-волонтери зможуть внести зміни на краще в життя дітей-сиріт шляхом стимулювання їхнього розвитку та надання відповідної допомоги.
Деякі етапи розвитку дитини
Емоційне здоров’я
Діти повинні відчувати, що їх люблять і що вони не є одинокими, а належать до певної групи.
Волонтери мають бути надійними. Діти мають відчувати добробут. Посміхайтесь до них, вітайте їх разом та кожного окремо. Найдрібніша річ, яку вони навчились робити самотужки, має позитивно відзначатися. Люди докладають більше зусиль за умови позитивного стимулювання, а не негативного.
Дисципліна має бути суворою, логічною, зрозумілою та збалансованою. Дитину не можна бити або кричати на неї. Дитина, яка відмовляється припинити крик, має бути ізольованою від інших (закрита кімната, або відокремлена її частина) до тих пір, доки сама не перестане плакати. Мотивація таких дій вихователя має бути чітко роз’яснена дитині. Та дитина, що б’є інших або забирає в них іграшки, також має бути ізольованою в іншу частину ігрової кімнати. Ідея таких дій полягає в наступному: доки дитина не зможе правильно гратися в колективі, вона не зможе бути частиною цього колективу. Проте, незважаючи на сувору дисципліну, дитина, яка завинила має відчувати, що її люблять. Слід пам’ятати, що в дисциплінарних заходах немає нічого спільного з любов’ю.
Волонтери мають бути чутливими, дружніми та люблячими. Вони мають залишати свої власні проблеми перед дверима дитячого притулку. Вони приходять туди для того, щоб дати дітям додаткову увагу та стимулювання, тому волонтери мають бути позитивно налаштованими та спокійними. Лише в люблячому оточенні індивід може навчитися любити інших навколо себе, намагатися виправити себе та набути позитивного світосприйняття. Ця істина є однаково вірною і для новонароджених, і для дорослих.
Волонтери мають з розумінням ставитися до своїх дітей. В процесі свого розвитку діти часто “відкочуються” назад, мають емоційні зриви, стають дратівливими. Це може проявлятися криком, грубою поведінкою, відмовою від їжі тощо. Волонтери не повинні проявляти власних емоцій, проте залишатися спокійними, сприятливими та турботливими, весь час пам’ятаючи про суворість.
Волонтери мають бути врівноваженими. Діти повинні знати, що кожний з волонтерів завжди є спокійним та турботливим. Діти мають розраховувати на певний тип поведінки дорослих та відповідну реакцію з їхнього боку.
Фізична рухливість
Усі люди повинні вміти користуватися своїми великими м’язами. Без цього людина є надзвичайно обмеженою.
В дітей та підлітків має бути достатньо часу для тренування їх ніг, рук, шиї та ступнів. Дитина має вміти рухати ногами, діставати необхідні їй речі, кидати речі, бити їх, тримати. Більш дорослі діти мають вчитися спочатку сидіти, потім повзати, а згодом і стояти. Після того, як дитина навчилась стояти, вона має вчитися бити по м’ячу ногами, тримати, штовхати, підбирати, хапати, переносити речі. Якщо ж внаслідок своєї вади дитина не може повзати або стояти, волонтери мають допомогти їй навчитися сидіти так, щоб дитина могла вільно використовувати свої руки для діставання об’єктів, їх перекладання, кидання тощо.
Розвиток малих м’язів є таким же важливим, як і розвиток великих. Дитина повинна мати можливість дотягуватись до об’єктів, які вона бачить, триматися за палець волонтера, брати речі. Більш дорослі діти починають поєднувати різноманітні об’єкти, користуються кольоровими олівцями, малюють на папері, ловлять, кидають та б’ють великий резиновий м’яч, граються з частинами великих головоломок, переливають воду з одного контейнера в інший.
Розвиток органів чуття
СЛУХ. Постійно говоріть з дитиною. Співайте самі або включайте для неї музику. Імітуйте звуки, що робить дитина. Читайте дитині невеличкі віршики, які мають гарну риму та музичні інтонації. Кожного разу, як волонтер підходить до дитини, він повинен називати своє ім’я. Крім того, волонтер має звертатися до самого себе за власним ім’ям для того, щоб дитина могла ідентифікувати особу не лише візуально, але й за звуком. Також якомога частіше слід вживати власне ім’я дитини.
ЗІР. Вчіть дитину розглядати об’єкти на сторінках книжок: слоник, півник, собака тощо. Використовуйте свій звичайний одяг для демонстрації різних кольорів. Грайте в ручні ігри. Робіть цікаві рухи руками в повітрі так, щоб дитина могла спостерігати за вашими руками. Коли дитина рухається, знайдіть який-небудь об’єкт, назвіть його та попросіть дитину описати його. Постійно називайте об’єкти навколо вас, кольори та малюнки в книжках.
МОВЛЕННЯ. Волонтери мають постійно розмовляти з дитиною та позитивно відповідати на усі звуки, що вимовляє дитина. Коли мова стає чіткішою, усі звуки, що нагадують нормальні українські слова, мають схвально сприйматися вихователем та повторюватись. Волонтер має постійно ставити дитині прості питання, навіть якщо дитина ще не в змозі на них відповісти. Потім волонтер має задавати ті самі питання самому собі та давати на них відповідь. Цей метод сприяє розвитку мовного спілкування.
ДОТИК. Дитину треба вчити розрізняти м’які, гладкі, круглі об’єкти. Коли дитина торкається предметів з різною поверхнею та структурою, волонтер має пояснювати, що це і з чого вони зроблені. Це допомагає розвинути тактильну чутливість та розширює словник дитини.
Стимуляція розумового розвитку
Діти потребують стимуляції їхнього розумового розвитку від самого моменту народження, незважаючи на майбутній довготривалий процес пізнання.
Це означає, що дітей треба вчити якомога більшій кількості різноманітних речей відповідно до рівня їхнього розвитку. Волонтер має постійно розмовляти з дитиною, ставити їй питання навіть ще до того, як дитина буде здатною повністю зрозуміти питання та дати на нього відповідь. Книжки слід читати раніше, ніж дитина навчиться розрізняти різні малюнки на сторінці. Таке читання збільшує словниковий запас дитини, стимулює зір, закладає першу основу в подальшому розумінні концепції книги (на першому етапі під терміном “читання” розуміється називання об’єктів, кольорів та малюнків на сторінці з подальшим розпитуванням дитини, що й де знаходиться на сторінці). Крім того, читання сприяє розвитку мовлення. У віці одного року або біля того, звичайно за умови, що дитина готова до цього, волонтер може поступово вводити літери та цифри. Дуже важливим є рахування вголос для дитини.
Дітей треба водити на прогулянки та показувати різноманітні нові місця. Їх треба просити дивитися на об’єкти та спостерігати за ними. Цим об’єктам треба давати імена.
Далі подається спеціальна інформація та рекомендації щодо дій волонтерів, спрямованих на розвиток дитини по чотирьох основних етапах, поданих вище. Робота над усіма чотирма етапами проводиться одночасно. Успіх в чомусь одному сприяє успішному просуванню в іншому. Розвиток дитини складається з багатьох маленьких кроків. Роль волонтерів полягає в тому, щоб допомогти дитині розвинутися якомога повніше. Під час занять волонтер не повинен залишати дитину без нагляду. Це є перше правило, яке завжди треба пам’ятати.
- Дитина лежить на спині
Коли волонтер починає гратися з дитиною або робити вправи, скеровані на її стимуляцію, він має перевернути дитину на спину або взяти її на руки. Коли дитині виповнюється кілька місяців, вона вже може гратися зі своїми пальчиками на ногах, спостерігати за власними руками та пальцями, намагатися дотягнутися до об’єктів, що висять над нею. Також, лежачи на спині, дитина може бачити та спілкуватися з волонтером – а це є надзвичайно важливим.
Волонтер має сприяти дитині в її іграх з власними ручками та ніжками. В залежності від того, яку вроджену ваду має дитина, вона може потребувати подушки або валика, покладених під її спину. Це дозволить дещо підняти її торс таким чином, щоб дитина могла бачити власні руки.
Коли дитина лежить на спині, дайте їй м’яке кільце, брязкальце, невеличку іграшку – так, щоб дитина могла тримати та роздивлятися їх. Тримайте іграшки над дитиною, але достатньо близько, щоб дитина могла їх торкатися й розкачувати. Грайтеся в ладоньки та в інші двосторонні ігри на координацію. Допоможіть дитині навчитися хлопати в долоні. Говоріть з дитиною, називайте речі, співайте, смійтеся разом з дитиною, а головне – посміхайтеся. Волонтер має часто нахилятися до дитини так, щоб вона могла близько бачити його обличчя та намагатися торкнутися його.
В разі, якщо дитина є сліпою, використовуйте тактильну стимуляцію. Кладіть речі прямо їй в руки, тримайте об’єкти перед руками після того, як дитина зрозуміє, де є даний об’єкт та спробує дотягнутися до нього. Постійно говоріть з дитиною. Називайте об’єкти та речовину, з якої вони зроблені. Давайте дитині самі різноманітні об’єкти: м’які, гумові, гладкі, тверді тощо. Волонтер – це очі дитини, отож він має словами описувати усе, що дитина робить та чого торкається.
- Дитина лежить на боку
Коли дитина лежить на боку, вона може більш вільно використовувати свої руки. Допоможіть дитині зручніше лягти на бік, підклавши подушку або валик так, щоб дитина не перекочувалась на спину. Покладіть іграшку на відстань витягнутої руки від дитини так, щоб вона могла до неї дотягнутися. Похваліть дитину, коли вона зробить це. В разі потреби – допоможіть.
- Дитина лежить на животику
Покладіть дитину на животик для того, щоб зміцнити її м’язи рук, плечей та шиї. Коли дитина напружує м’язи шиї та плечей, намагаючись тримати голівку лежачи на животі, допоможіть їй в разі потреби. Для цього достатньо просунути свої руки під плечі дитини. Покладіть перед дитиною ляльку або будь-який інший яскравий об’єкт. Це має спонукати дитину піднятися на витягнутих руках для того, щоб краще роздивитися об’єкт або дотягнутися до нього. Якщо дитина лежить на животі і протягом певного часу може утримувати себе на витягнутих руках – вона вже в змозі протягнутися й взяти її. Але для того, щоб взяти який-небудь предмет, дитині необхідно перенести вагу тіла на одну руку. Інколи дитина надто різко переносить вагу і просто падає на спину. Якщо таке стається – просто покладіть дитину знову на животик. З часом вона навчиться переносити свою вагу на одну руку, не падаючи при цьому, і дотягуватися до предметів, що її зацікавили. Ці рухи є надзвичайно важливими для подальшого навчання повзати. Постійно підтримуйте й хваліть дитину. Вона намагатиметься робити речі краще, якщо зрозуміє, що це вам подобається. Але не треба тиснути на дитину, яка ще не досягла певного етапу розвитку. Якщо дитина не проявляє ніякої зацікавленості або здатності підтримувати запропоновану вами діяльність – облиште це і поверніться до попередньої стадії.
Перекачування з живота на спину зазвичай проявляється перед перевертанням. Такі вправи допомагають дитині використовувати по черзі обидві руки. Перекачування з живота на спину випереджує перевертання зі спини на живіт.
Перекачування з живота на спину зазвичай проявляється перед перевертанням. Такі вправи допомагають дитині використовувати по черзі обидві руки. Перекачування з живота на спину випереджує перевертання зі спини на живіт.
Якщо дитина може простягнути одну руку за іграшкою, спираючись на іншу руку, – вона готова перевертатися з живота навколо себе. Для того, щоб взяти іграшку, дитині треба по черзі перенести вагу з однієї руки на іншу та зробити круговий рух тілом. Таким чином, перевертання зміцнює м’язи рук та плечей.
- Дитина сидить
Коли дитина відчуває себе достатньо готовою, вона намагається сидіти. Допоможіть їй, використовуючи спеціальне дитяче сидіння. Якщо внаслідок фізичної неповноцінності в дитини виникають труднощі з сидінням, спробуйте усадити дитину, підклавши їй під спину та голову подушки. Під час сидіння руки дитини є вільними і вона може тягнутися до предметів, які її зацікавили. Для нормального розвитку основних моторних функцій необхідна двостороння координація. Це важливо для ефективного використання обох рук. Сидіння є важливим для подальшого розвитку координації рухів руками. Крім того, в сидячому положенні волонтерові набагато легше займатися вправами для розумового розвитку дитини та стимуляції її органів чуття. Якщо руки в дитини вільні, їй легше вчитися брати та піднімати речі, тримати та кидати їх. Сядьте навпроти дитини та давайте їй іграшки або поставте перед нею невеличкий столик та розставте іграшки на ньому. Дайте дитині в руку який-небудь музичний інструмент, кубики або інші невеличкі предмети, які добре поєднуються разом. Чудовим розвиваючим інструментом є іграшки, в яких знімається верх, або які можна розібрати на окремі деталі. Мета таких дій – навчити дитину використовувати обидві руки для того, щоб скласти або розібрати щось, взяти предмет, кинути його та підняти знову. Хлопання по іграшкам сприяє розвитку м’язів та координації рухів, а в майбутньому стане на пригоді для ефективного використання обох рук та пальців. Також волонтер може посадити дитину собі на коліна, сперши її на свій живіт. В такому положенні руки дитини також залишаються вільними і вона може гратися з оточуючими предметами або власними пальцями. Крім того, така позиції – ідеальний час для читання.
- Дитина повзає
Дитина може почати повзати після того, як ви покладете її на живіт. Вона підтягує коліна та утримує себе, спираючись на руки та коліна. Якщо логічний наступний крок затримується, спробуйте допомогти дитині, підтримуючи її за стегна. Мало помалу дитина, стоячи в такому положенні, відчує себе достатньо сильною і впевненою для того, щоб підняти одну руку та взяти іграшку. Після цього вона почне рухатися вперед. Волонтер може допомогти дитині, надихаючи її на продовження руху, тримаючи іграшку прямо перед нею так, щоб дитині залишалось тільки зробити крок і взяти її. Після того, як дитина взяла іграшку, її обов’язково треба похвалити та дати погратися з іграшкою.
- Дитина стоїть
Дітей треба спонукати до стояння. З більшістю дітей цей процес проходить доволі природно, але наявність вроджених вад може затримати це. Тренування дитини для переходу від сидіння до стояння полягає в наступному: посадіть її на низький стільчик так, щоб ноги дитини торкались підлоги. Простягніть дитині руки, щоб допомогти їй встати. Або поставте перед нею інший стілець так, щоб вона могла встати самотужки, тримаючись за нього. Коли дитина навчилась впевнено стояти, вона може використовувати свої м’язи для того, щоб штовхати та кидати предмети. Дозволяйте їй відкривати та закривати дверці серванту, возити іграшку на колесах, штовхати коробку по підлозі. Такі вправи сприятимуть постійному розвитку спритності та контролю за м’язами. Така діяльність, як пересипання піску або переливання води з одного контейнера в інший, непогано стимулює розвиток дитини. Для виконання такого ж завдання дитина може використовувати велику ложку або ж лопатку. Дитині треба дозволяти ходити вверх та вниз сходами, бігати, плигати й стрибати. Всі ці вправи повинні виконуватися під наглядом волонтерів.
Інші види стимулюючої діяльності
- Читайте дитині простенькі вірші та співайте пісні. Це є надзвичайно сприятливим для розвитку мовлення та розпізнавання звуків.
- Кладіть іграшки в коробку і дозволяйте дитині витягати їх звідти. Опишіть ці іграшки простими словами. Якщо дитина вже досить доросла, попросіть її саму описати іграшки, які вона бачить. Під час гри використовуйте іграшки та предмети з різних матеріалів та різною будовою.
- Дайте дитині іграшки, що можна складати одну на одну. Така гра навчить дитину співвідносити розміри та форму і покращить моторні функції.
- Грайте в ігри на відгадування: сховайте за спиною улюблену іграшку дитини та попросіть її відгадати, яку саме іграшку ви ховаєте. В разі потреби волонтер може давати дитині певні підказки. Мета подібних ігор полягає в тому, щоб змусити дитину вголос висловлювати свої думки та бажання й навчити її розуміти те, що іграшка нікуди не ділась, навіть, якщо дитина її не бачить.
- Читайте дитині книжки. Вказуйте на малюнки на сторінках книг, називайте намальовані предмети, кольори, дії. Просіть дитину саму вказувати на певні об’єкти. Збільшуйте словниковий запас шляхом постійного повторення слів, що найчастіше зустрічаються.
Але найважливішим є те, що ви маєте постійно розмовляти з дитиною. Називайте її ім’я. Називайте себе на ім’я. Повторюйте звуки, що вимовляє дитина. Повторюйте разом з нею прості слова. Використовуйте знакову заміну мови під час роботи з дітьми, які мають порушення слуху. З такими дітьми можете спробувати наступне: візьміть руку дитини та піднесіть до свого рота під час розмови. Потім візьміть цю ж руку і піднесіть її до рота дитини продовжуючи в цей час говорити. Попросіть дитину повторити. Коли дитина стане дорослішою, цю вправу можна ускладнити: покладіть одну її руку собі на шию, іншу на рота – і говоріть. При цьому дитина повинна дивитися на вас. Потім перекладіть руки на саму дитину і попросіть, щоб вона повторила сказане вами. При роботі зі сліпими дітьми використовуйте тактильну чутливість та голос для озвучення своїх дій.
Пам’ятайте, що завдання волонтерів полягає в наданні емоційної допомоги та сприянні фізичному розвитку дитини, стимуляції її органів чуття й попередження розумового відставання.
Приклади виготовлення іграшок для дітей з дитячого будинку
Якщо фінансування для закупівлі книжок, іграшок та іншого обладнання бракує, найнеобхідніші в процесі навчання речі можна зробити самотужки.
Книжки: виріжте з журналів великі, але не згруповані малюнки та наклейте їх на картон.
Геометричні іграшки: можна використовувати паперові або пластикові стаканчики різних розмірів.
Ляльки: візьміть шкарпетку та наповніть її ватою або будь-яким іншим м’яким матеріалом. Зробіть їй талію перетягнувши мотузкою. З інших частин шкарпетки зробіть руки й ноги. Замість очей і рота нашийте ґудзики.
Матеріал для ліплення: замість пластиліну або глини можна використовувати саморобну суміш: 1 склянка борошна, 1 склянка води, ½ склянки солі, 1 чайна ложка олії, будь-який барвник. Все це розмішати й поставити на великий вогонь. Готувати постійно помішуючи, доки маса не набуде однорідної клеєподібної структури. Дайте їй охолонути. Отриману масу можна зберігати кілька тижнів в пластиковому контейнері або посуді, що щільно закривається.
Брязкальце: візьміть будь-який невеличкий порожній предмет, що щільно закривається або, принаймні, має отвір. Насипте всередину горох і закрийте або заклейте отвір скотчем.
Ігри в переливання: візьміть сухий пісок, горох або рис, столову ложку та кілька контейнерів і дайте все це дитині.
Розклад праці волонтерів
Волонтери мають відвідувати своїх підлеглих кожного дня з понеділка по п’ятницю. На мою думку, найефективніший розклад праці волонтерів передбачає дво- або тригодинне заняття з трьома-чотирма дітьми зранку та принаймні одну годину після обіду.
В ідеалі волонтери могли б залишатися з дітьми протягом всього академічного року. В разі необхідності заміни опікуна у певної дитини, я сподіваюсь, що кожен з волонтерів залишатиметься з дитиною принаймні протягом шести місяців. Для полегшення адаптації необхідно, щоб протягом двох тижнів обидва волонтери одночасно займались з дитиною. Така процедура полегшить процес розставання і дитині і волонтерові. За ці два тижні новий волонтер має навчитися всьому, що робив його попередник, запам’ятати, що вже пройдено з дитиною, а що ще ні, та, головне, що дитині подобається, а що ні, і в чому полягає її вада (в разі наявності). Треба докласти максимум зусиль, щоб дитина звикла до нового опікуна і не так важко перенесла їх зміну.
Переглянуто редакційною колегією I.B.I.S.: 15/02/2003
Синдром Вівера
(Weaver Syndrome)
О.П. Семененко
Лікар-генетик
Черкаського обласного перинатального центру
Синоніми:
- Weaver–Smith syndrome;
- WSS;
- Weaver–Like syndrome, included.
Основні діагностичні критерії:
- Макросомія.
- Прискорений розвиток скелету.
- Характерні, незвичні риси обличчя.
- Камптодактилія.
Клінічна симптоматика:
Зріст:
Прискорений розвиток починається на початку внутрішньоутробного періоду, причому збільшення ваги випереджає зріст. Великі при народженні діти мають швидкий темп росту і значно випереджаючий кістковий вік в грудному віці з перевагою кистьових центрів над фаланговими. В рідкісних випадках прискорення росту не відбувається до декількох місяців. У двох характерних випадках кінцевий зріст пацієнтів становив 209,5 см та 187 см.
Розвиток:
- Грубий голос.
- Затримка мовного розвитку проявляється “ковтанням” слів або дизартрією.
- Розумова відсталість при синдромі, як правило, легкого ступеню.
- Загальним для всіх пацієнтів є проблеми поведінки, низька концентрація уваги, дратівливість.
Краніофаціальні аномалії:
- Мікроцефалія.
- Пласка потилиця.
- Виражений гіпертелоризм.
- Епікант.
- Страбізм.
- Плоске перенісся.
- Великі вуха.
- Довгий фільтр.
- Відносна мікрогенія.
Скелет:
- Камптодактилія, що спричиняє здавлення пальців ніг.
- Широкі перші пальці.
- Тонкі глибокі нігті.
- Виступаючі пальцеві подушечки.
- Сколіоз.
- Кіфоз.
- Обмеження розгинання ліктьових і колінних суглобів.
- Еквіноварусні деформації ступнів.
- Гіпереластична шкіра.
- Тонке волосся.
- Пахові кили.
- Пупкові кили.
- Крипторхізм.
Поєднані аномалії:
- Вади серця.
- Короткі ребра.
- Нестабільність першого шийного хребця.
- Епілепсія.
- Кіста прозорої перетинки.
- Гіперваскуляризація в ділянці середньої і лівої задньої церебральних артерій.
- Нейробластома.
Етіологія:
Невідома. Більшість випадків спорадичні. Однак є повідомлення про легкі прояви у матерів, що мали синів із синдромом Вівера, що не виключає можливості аутосомно-домінантного зчепленого зі статтю успадкування або Х-зчепленого рецесивного типу успадкування.
Номер з каталогу МІМ:
277590 Weaver Syndrome; WVS.
Список літератури:
- Cole TRP, Dennis NR, Hughes HE. Weaver syndrome. J Med Genet 1992;29:332-337.
- Gorlin RJ, Cohen MM, Hennekam RCM. Syndromes of the Head and Neck. 4-th edition. Oxford University Press. 2001:413 (T11-5).
- Jones KL. Smith’s Recognizable Patterns of Human Malformation. 5th ed. Philadelphia: W. B. Saunders Company 1997:158,159-161.
Переглянуто редакційною колегією I.B.I.S.: 02/04/2008
Фенілкетонурія
(Phenylketonuria, PKU)
Любов Степанівна Євтушок
Зав. медико-генетичною консультацією
Рівненського клінічного лікувально-діагностичного центру
Фенілкетонурія – це спадкове захворювання, яке, при відсутності лікування призводить до розумової відсталості. 1 з 50-70 людей є носієм гена фенілкетонурії. Хоча ця хвороба не дуже поширена (1 дитина на кожних 8-13 тисяч новонароджених), вона потребує великих витрат. В США, наприклад, щороку витрачається кілька мільйонів доларів на лікування хворих дітей. Але навіть це не можна порівняти з тим горем, яке приходить в сім‘ю з народженням хворої дитини.
Фенілкетонурія – це спадкова хвороба, яка зумовлена дефектом гена ферменту фенілаланінгідроксилази, що знаходиться на довгому плечі 12 хромосоми (12q 22-24). Саме це і призводить до порушення обміну амінокислоти фенілаланіну – необхідної для життя амінокислоти, яку ми отримуємо з їжі.
“Феніл” – від слова фенілаланін (назва однієї з 20 амінокислот, які входять у склад білкової молекули).
“Кетон” – від слова кетони (продукти обміну цієї амінокислоти).
“Урія” – виділення продуктів обміну з сечею.
Порушення метаболізму фенілаланіну:
В нормі фенілаланін перетворюється на тирозин за допомогою ферменту гідроксилази фенілаланіну (ФФГ). Для цього перетворення необхідний тетрагідробіоптерин (ВН4). Він необхідний також для біохімічних процесів в ході синтезу нейромедіаторів – допаміну, норепінефріну, і серотоніну. В нормі рівень фенілаланіну в крові відповідає 180 mmol/l (3 mg/dl) або менше.
Причини підвищення рівня феніаланіну:
Існує кілька причин підвищення рівня фенілаланіну в крові (гіперфенілаланінанемія) (табл. 1). Тому, це відхилення потребує детального дослідження перед тим, як встановлювати конкретний діагноз для немовляти з гіперфенілаланінамією та призначати лікування. Нижче поданий перелік причин гіперфенілаланінамії та біохімічні показники для їх диференціації.
Таблиця 1.
Причини підвищення фенілаланіну.
|
Фенілкетонурія (ФКУ)
|
>1200
|
<250
|
Норма
|
Норма
|
Норма
|
|
ФКУ середньої важкості
|
600 – 1.200
|
<250
|
Норма
|
Норма
|
Норма
|
|
Гіперфенілаланінемія, не пов’язана із ФКУ
|
180 – 600
|
<250
|
Норма
|
Норма
|
Норма
|
|
Дефекти птерину
|
|||||
|
Дефіцит циклогідролази
|
180 – 1.200
|
<250
|
Норма
|
Аномальний
|
Аномальний
|
|
Дефіцит синтезу пірувол -тетрагідроптеріну
|
180 – 1.200
|
<250
|
Норма
|
Аномальний
|
Аномальний
|
|
Дефіцит дегідроптерін-редуктази
|
180 – 1.200
|
<250
|
Норма
|
Аномальний
|
Аномальний
|
|
Транзиторна гіперфенілаланінемія
|
180 – 840
|
<250
|
Норма
|
Норма
|
Норма
|
|
Тирозинемія І, галактоземія, хвороби печінки
|
180 – 600
|
>250
|
Підвищений рівень метіоніну
|
Норма
|
Норма
|
Дефіцит гідроксилази фенілаланіну:
Дефіцит активності ФФГ призводить до підвищення рівня фенілаланіну в крові. Ступінь підвищення залежить від ступеня ензимної недостатності. Класична форма ФКУ, яка в Сполучених Штатах та Європі трапляється з частотою 1:13.000, зазвичай дає при обстеженні такі показники: 1) концентрація фенілаланіну в крові 1200 mmol/l (20 mg/dl) і вище у новонароджених при грудному вигодуванні або вживанні суміші; 2) концентрація тирозину в крові менше 250 mmol/l (5 mg/dl); 3) проба на птерин у сечі, який вказує на недостатність ВН4, в нормі. При класичній формі ФКУ активність ФФГ печінки наближається до нуля. При м’яких формах ФКУ (атипова ФКУ) спостерігається рівень фенілаланніну в крові у межах 600-1200 mmol/l (10-20 mg/dl), нормальний або низький рівень тирозину, нормальна проба на птерин у сечі; на цьому фоні проявляється незначна резидуальна/залишкова активність ФФГ.
Приблизно 20-50% немовлят, у яких була виявлена гіперфенілаланінанемія під час скрінінгу новонароджених, мали стійку м’яко виявлену, не пов’язану з ФКУ гіперфенілаланінанемію (МГФ) з рівнем фенілаланіну в крові 180-600 mmol/l (3-10 mg/dl) та стійкою активністю ФФГ до 10%. МФГ вважалась не шкідливою, але, грунтуючись на результатах останніх досліджень, було висунуто припущення, що стійке підвищення фенілаланіну в крові вище 360 mmol/l (6mg/dl) може знижувати показник розумового розвитку IQ. Інші дослідження, навпаки, показують, що стійке підвищення фенілаланіну в крові до рівня 600 mmol/l (10mg/dl) не викликає ніяких проблем. Існує розбіжність в поглядах на те, чи призначати обмежуючу дієту немовлятам з рівнем фенілаланіну 360-600 mmol/l (6-10 mg/dl). У деяких клініках дієтичне лікування призначається дітям з рівнем фенілаланіну вище 480 mmol/l (8mg/dl).
Порушення, пов’язані з тетрагідробіоптеріном:
Порушення синтезу та переробки ВН4 призводять до виникнення гіперфенілаланінанемії. Важливо відмітити, що діти з цим відхиленням страждають на прогресуючу, часто у важкій формі, неврологічну деградацію, якщо їм помилково ставлять діагноз класичної ФКУ і лікують тільки дієтою із зниженим вмістом фенілаланіну. Недостатність ВН4 обмежує перетворення фенілаланіну на тирозин, а пов’язане з діяльністю ЦНС перетворення тирозину в DOPA та триптофану в 5-гідрокситриптофан. Таким чином, ці порушення призводять до підвищення фенілаланіну та порушень у синтезі нейромедіаторів. Рідко трапляються випадки, коли недостатність ВН4 є тільки периферійною і не впливає на синтез медіаторів в ЦНС, де їх рівень залишається в нормі. За останні роки в деяких країнах був налагоджений збір даних з діагностики та лікування цього рідкісного захворювання (1:1.000.000 або 1% від усіх новонароджених з неонатальною гіперфенілаланінанемією). Лікування передбачає введення додаткового ВН4 і медикаментів, які підвищують рівень нейромедіаторів.
Транзиторна гіперфенілаланінанемія:
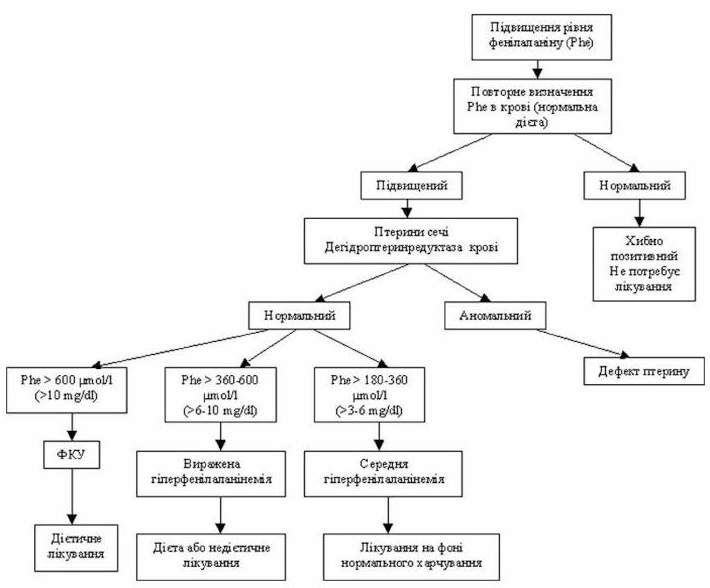
Гіперфенілаланінанемія, виявлена під час скрінінгу новонароджених, може мати тимчасовий характер. Це, як правило, відносно невисоке підвищення фенілаланіну, що спостерігається у перші місяці життя і не потребує спеціальної терапії. У деяких випадках гіперфенілаланінанемія є вторинною як наслідок тимчасової гіпертирозинанемії. Описані випадки більш важких форм тимчасової гіперфенілаланінанемії, при яких спочатку виникала необхідність в лікуванні (рівень 480-840 mmol/l або 8-18 mg/dl). Згодом видужання наставало само по собі в процесі росту дитини. На малюнку 1 показано алгоритм лікування при неонатальній гіпераланінемії.
Малюнок 1.
Тирозинемія І-го типу (спадкова тирозинемія):
Гіперфенілаланінанемія часто трапляється при тирозинемії І-го типу. Це симптом вторинного характеру. Очевидно, він виникає внаслідок важкого метаболічного ураження печінки. Одночасне визначення рівнів фенілаланіну та тирозину дає змогу визначити результатом тирозинемії чи ФКУ є гіперфенілаланінанемія.
Галактоземія та інші захворювання:
Галактоземія та інші захворювання, які викликають дисфункцію печінки, також можуть спричинити підвищення фенілаланіну в крові вторинного характеру. У таких випадках гіперфенілаланінанемія супроводжується підвищенням в крові рівня метіоніну та тирозину. Щоб виявити такі вторинні причини гіперфенілаланінанемії, необхідно провести подальше обстеження дитини та знати її клінічний фенотип.
Як це впливає на дитину?
Внаслідок порушення обміну фенілаланін накопичується в крові і тканинах і стає “отрутою” для організму дитини, що росте.
Діти, які народилися з фенілкетонурією, в перші кілька місяців здаються цілком здоровими. Але, якщо лікування не розпочате, вони через 3-5 місяців втрачають набуті навички, інтерес до оточення. А коли їм виповнюється рік, вони вже мають розумову відсталість.
Діти з ФКУ мають знижений м’язовий тонус, часто є дратівливими. Їх тіло і сеча мають характерний мишачий запах або запах плісняви. Шкіра у них буває суха, часті дерматити. В деяких випадках виникають судоми, характерні “кивки”. Як правило, хворі діти добре розвиваються фізично, мають надмірну вагу і світліше волосся, ніж їх родичі.
Генетика ФКУ (яким чином передається ця хвороба?)
Фенілкетонурія є спадковою хворобою. Вона проявляється лише тоді, коли обидва батьки мають ген хвороби і передають його дитині. Такий тип успадкування називається аутосомно – рецесивним. Якщо в одній клітині є один нормальний ген і один ген фенілкетонурії, то така людина називається носієм. Вона не має ніяких проявів хвороби, але може передати хворобливий ген своїм нащадкам (Схема № 1).
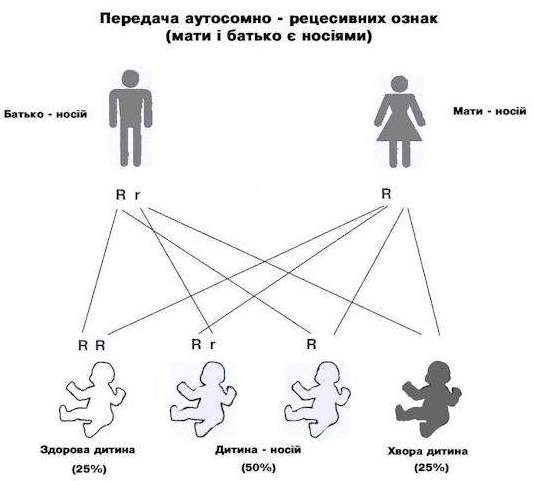 Схема № 1.
Схема № 1.
Якщо обидва батьки є носіями, то існує 25% шансів, що кожен з них передасть дефектний ген дитині, викликаючи таким чином народження хворої дитини. Є також 25% шансів (1 з 4), що вони передадуть здорові гени і дитина народиться цілком здоровою. І, нарешті, є 50% шансів, що у дитини буде один нормальний ген і один ген фенілкетонурії. В цьому випадку дитина буде носієм, як і її батьки.
Чи є можливість діагностувати ФКУ?
Так. За допомогою спеціального тестування крові (потрібно лише кілька крапель, які висушують на фільтрувальному папері) можна діагностувати хворобу, коли дитина має лише 5-6 днів від народження і знаходиться в пологовому будинку. Проби крові аналізуються на рівень фенілаланіну і визначається причина його підвищення, якщо таке є.
Помилково позитивні результати скрінінгу новонароджених – це тимчасові відхилення від норми, причиною яких є не порушення обміну речовин, а інші фактори, наприклад, недоношеність. Вони викликають в сім’ях тривогу. Щоб полегшити переживання батьків, необхідно пояснити їм результати аналізів та необхідність проведення повторного обстеження.
Існує також тест сечі з трихлорним залізом, але він дає менш надійні результати. Причина полягає в тому, що в перші дні життя фенілаланін не може накопичуватись на рівнях, які необхідні для отримання позитивного результату тесту.
Молекулярна діагностика (діагностика на рівні гена) можлива як для пренатальної (допологової), так і постнатальної (післяпологової) діагностики хвороби.
Обстеження дитини з фенілкетонурією:
Обстеження дитини з ФКУ включає встановлення кількісних рівнів амінокислот в плазмі та сироватці при особливій увазі до фенілаланіну та тирозину, а також збір проб крові та сечі на аналіз птеріну. Паралельно з цим батьків інформують про особливості ФКУ та подібних захворювань та надають консультацію з генетичних питань. У деяких випадках, особливо коли необхідність введення дієти стає більш нагальною, ніж видавалось після перших аналізів, доцільно зробити аналіз на ФФГ – генотип, щоб переконати батьків в точності діагнозу і в необхідності тривалого медичного нагляду. Визначення рівня фенілаланіну в крові кожного з батьків повинно бути зроблене на початку обстеження дитини. Рідко трапляється так, що у когось з батьків підвищений рівень фенілаланіну.
Лікування фенілкетонурії:
З того моменту, як обстеження показало, що рівень фенілаланіну у дитини вимагає розпочати лікування (в багатьох клініках це 480 mmol/l або 8mg/dl), вводиться дієта з обмеженим вмістом фенілаланіну. Якщо аналізи на птерин показали відхилення від норми, може виникнути потреба в додатковому прийомі ВН4 та медикаментів, які збільшують рівень нейромедіаторів.
Принцип лікування фенілкетонурії – спеціальна дієта, тобто лікувальне харчування. Він полягає в обмеженні поступлення в організм дитини фенілаланіну з їжею. Якщо розпочати дієту з 10 – 20-го дня життя, то це запобігає розвитку розумової відсталості.
Фенілаланін входить у склад всіх білкових продуктів. Тому із раціону харчування хворого необхідно виключити ті продукти, які мають багато білка. До них відносяться м‘ясо, риба, яйця, молоко та молочні вироби, хліб.
Лікувальне меню хворого, в основному, складають продукти рослинного походження – овочі, фрукти, ягоди, зелень. Але організм дитини не може формуватися при такому дефіциті білка. Тому в раціон дитини додають спеціальні лікувальні суміші, в складі яких зменшена кількість або повністю видалений фенілаланін, такі як Лофеналак, Феніл-фрі, Нофелан та інші.
Розрахунок білкового компоненту їжі для хворої дитини повинен робити лікар.
Період грудного віку:
Кожне годування розпочинається з пляшечки з амінокислотним додатком. Після того, як прорахована необхідна кількість рідини випита, дитина отримує важливий для життя фенілаланін з грудного молока матері. При ФКУ споживається невелика кількість натуральної їжі. Грудне молоко містить відносно малу кількість фенілаланіну і є найбільш адаптованим для немовляти, тому мам заохочують до грудного вигодовування. Якщо жінка не вигодовує дитину грудним молоком, дитині дають невелику кількість суміші додатково до амінокислотної добавки. У процесі росту дитини дієта доповнюється крупами без вмісту протеїну і точно виваженою кількістю овочів та фруктів. З ростом дитини і розширенням її раціону, батьки матимуть час дізнатись, як поступово ускладнювати дієту.
Щоденна необхідність вживати амінокислотні добавки крім звичайної їжі може стати причиною конфлікту і призвести до відчаю, злості, сліз, як у дітей, так і у батьків.
Схема введення продуктів прикорму для грудної дитини така ж, як і у здорових. Спочатку вводяться соки, потім фруктове і овочеве пюре. В раціоні хворої дитини необхідна сагова каша або безбілкова крупа. З віком раціон розширюється (вегетаріанські страви, безбілковий хліб).
Дитинство та підлітковий вік:
Діти та підлітки з ФКУ вважають, що для них вибір їжі дуже обмежений. Менших дітей вчать нічого не їсти і навіть не пробувати без дозволу батьків. Звичайну їжу необхідно точно зважувати до грама і складати меню на день. Три або чотири рази на день треба вживати амінокислотні добавки до їжі. Із вживанням добавок проблем у більшості випадків не виникає, за виключенням тих випадків, коли хворий негативно реагує на їх смак чи запах. Важливо, щоб усі, хто спілкується з дитиною, знали про ФКУ достатньо для того, щоб не дати дитині не ту їжу або не в тій кількості. Важливо також проінформувати друзів та родичів, вихователів у дитсадку, осіб у школі, які відповідають за догляд за дитиною.
Амінокислотні добавки, розрахунок дієти, спеціальні продукти без вмісту протеїну необхідно мати з собою на усіх виїздах та в подорожах. На ринку починають з’являтись нові форми, альтернативні амінокислотним добавкам у порошку. У спресовану вигляді чи в капсулах вони займають менше місця, і можуть вживатись додатково або замість порошку під час подорожей або на вечірках.
Оскільки дотримання дієти має бути дуже суворим і пов’язане з великою кількістю розрахунків та вимірів ваги, у батьків та дітей з ФКУ часто розвивається сильне відчуття взаємозалежності. Важливо навчати дітей та підлітків усьому, що пов’язане з їхнім станом, щоб вони поступово ставали більш обізнаними і здатними самостійно давати собі раду. Перед сім’єю та найближчим оточенням дитини стоїть завдання забезпечити такі умови, при яких дитина виросте незалежною та розвине у собі нормальну самооцінку.
ФКУ є непомітною інвалідністю. При порушенні дієти недуга проявиться з новою силою через деякий час. Необхідно надати інформацію вчителям, які ведуть уроки кулінарії у школі. Дітям, хворим на ФКУ, необхідно дати можливість отримати практичні знання з самостійного приготування спеціальної їжі.
Дівчаток-підлітків з ФКУ необхідно рано проінформувати про контрацепцію. Особливо сувора дієта є необхідною як перед, так і під час вагітності. Вагітність необхідно планувати.
ФКУ сама по собі не впливає на вибір навчального закладу. Однак, якщо навчання чи майбутня професія будуть такими, при яких важко дотримуватись дієти, рекомендується від них відмовитись. Хворих на ФКУ звільняють від проходження військової служби через необхідність спеціальної дієти.
Дорослі з ФКУ:
Батьки повинні усвідомлювати свою велику відповідальність і забезпечити умови існування, при яких дитина залишатиметься здоровою. Необхідно ретельно виконувати рекомендації по дієтлікуванню дитини, щоб забезпечити її нормальний розвиток.
До недавнього часу діти з ФКУ отримували лікування обмежуючою дієтою тільки в дошкільний період, оскільки вважалось, що з настанням шкільного віку розвиток мозку припиняється, і загроза його ушкодження через надлишок фенілаланіну минає. Однак останні дослідження показують, що багато дітей, які припинили дієтотерапію, мають нижчий показник IQ і гірші показники в навчанні, ніж ті, що залишились на спеціальній дієті. В деяких дослідженнях описані випадки неврологічних порушень, аномалій мозкової діяльності, що впливають на уяву, проблеми психічного характеру у пацієнтів, які припинили дієту в ранньому шкільному віці і ніколи не перебували під належним наглядом спеціалістів з метаболічних захворювань. Виходячи з цього, хворим на ФКУ рекомендовано залишатись на обмежуючій дієті протягом усього життя та регулярно проходити на належному рівні огляд з приводу метаболічних захворювань.
Хоча рівень фенілаланіну, який рекомендують підтримувати, та частота проведення аналізів крові можуть відрізнятись у різних клініках, існують стандартизовані інструкції з дієти при захворюванні на ФКУ, розроблені британськими лікарями. Вони рекомендують розпочинати дієтотерапію не пізніше, ніж протягом перших 20-ти днів життя для усіх немовлят, в яких рівень фенілаланіну постійно становить вище 400 mmol/l (6.7mg/dl), підтримувати фенілаланін на рівні 120-360 mmol/l (2-6 mg/dl) в ранньому дитинстві та на рівні 480 mmol/l (8 mg/dl) у шкільному віці. Усвідомлюючи те, що, з ростом дитини з дотриманням суворої дієти виникають труднощі, пропонується підтримувати фенілаланін на рівні не вище 700 mmol/l (12 mg/dl), але навіть при такій концентрації у підлітків і дорослих виникають труднощі розумового плану в прийнятті рішень.
Дослідження у Норвегії та інших країнах показали, що сувора дієта має позитивний вплив і на тих дорослих, які ніколи до цього не лікувались від ФКУ.
Кількість дорослих молодих людей, які проходять лікування з раннього дитинства, зростає. Деякі з них дотримуються дієтичного харчування, інші – споживають звичайну їжу відповідно до тих рекомендацій, які існували до середини 80-их років. Є також такі, хто повернувся до дієти після різних за часом періодів звичайного харчування. Хворі, які обрали дієтичне лікування, зазначають, що їх стан покращується, коли вони утримують низький рівень сироваткового фенілаланіну.
ФКУ не є обмеженням для шлюбу, спільного проживання, сімейного життя. Але молоді люди повинні усвідомлювати, що їх діти будуть носіями гена ФКУ. Це не означає, що вони обов’язково захворіють на ФКУ, оскільки захворювання передається від обох батьків.
Контроль за лікуванням:
Правильність дієтлікування ФКУ підтверджується визначенням рівня фенілаланіну в крові. На фоні дієтлікування він не перевищує 4-8 мг%.
Частота проведення моніторингу крові теж різна, але британські медики рекомендують робити аналізи щотижня для дітей до 4-х років, кожні 2 тижні для дітей 4-10-ти років і щомісяця після 10-ти років. У деяких клініках прийнятий менш напружений графік моніторингу. Зазвичай, немовлята проходять обстеження щотижня поки рівень фенілаланіну в них не знизиться до 120-360 mmol/l (2-6 mg/dl). Після цього вони здають аналізи щотижня протягом перших 6-ти місяців життя, раз у два місяці – до 1 року життя, кожні 3-4 місяці – до 5-ти років і раз у півроку – на протязі усього життя. Рівень фенілаланіну визначається щотижня за допомогою аналізів крові, взятої батьками з проколу в пальчику дитини і висушеної на фільтрувальному папері. Старші діти, підлітки та дорослі теж беруть пробу крові самі у себе з проколу в пальці.
Контроль за лікуванням, фізичним та розумовим розвитком дитини здійснюють лікар-генетик, дитячий психіатр, психолог. У періоди частих інфекційних захворювань може виникнути потреба частіше перевіряти рівень фенілаланіну в сироватці крові.
Щеплення дітям проводять за звичайним графіком.
Материнство і ФКУ:
Коли жінка з фенілкетонурією вагітніє, існує високий ризик мікроцефалії, вроджених вад серця, розумової відсталості у її дитини, бо мозок ще ненародженої дитини пошкоджується ненормальним обміном речовин матері. Було відмічено високий показник спонтанних абортів.
Однак розумовій відсталості дитини можна запобігти. Дуже важливо майбутній матері знову розпочати дієтлікування і контролювати рівень фенілаланіну в крові перед зачаттям і в період вагітності щотижня. Дівчина – підліток повинна готуватися до майбутнього дорослого життя завчасно.
Дані літератури свідчать, що при дотриманні дієти та компетентному біохімічному контролі для підтримання рівня фенілаланіну на показниках 120-360 mmol/l протягом вагітності, народжуються здорові діти.
Номер з каталогу МІМ:
261600 Phenylketonuria; PKU.
Література:
- Frances E. Dougherty, Harvey L. Levy. “Phenylketonuria”. Devision of Genetics, Children’s Hospital and Department of Pediatrics, Harvard Medical School, Boston, MA 02115, USA.- Annales Nestle 1998, 56: 83-93.
- William L. Nyhan, M.D., Ph.D., Nadia A. Sakati, M.D. “Diagnostic Recognition of Genetic Disease”. Lea & Febiger, Philadelphia, 1987, 100-105.
Переглянуто редакційною колегією I.B.I.S.: 05/02/2004
Дивіться також:
- Продукти з низьким вмістом фенілаланіну
- Низькобілкові продукти харчування (ФКУ) виробництва Польщі
- Кулінарні рецепти для осіб з низькофенілаланіновою дієтою
- Досвід діагностики та лікування хворих на фенілкетонурію, виявлених по програмі скринінгу
- З досвіду лікування фенілкетонурії при пізній діагностиці в Одеському ММГЦ
- Фенілкетонурія (інформація для батьків)
З досвіду лікування фенілкетонурії при пізній діагностиці в Одеському ММГЦ
(Phenylketonuria, PKU)
З.М. Живац
кандидат медичних наук,
завідуюча Одеським міжобласним медико-генетичним центром
В Одеському міжрайонному медико-генетичному центрі (ММГЦ) у даний час на диспансерному обліку і дієтотерапії гідролізатами білка нараховується 18 дітей, що страждають на фенілкетонурію (ФКУ).
Усі випадки пізно діагностовані у віці дітей від 7,5 місяців до 5 років. З підозрою на ФКУ діти вибиралися традиційними методами в групі з затримкою психомоторного розвитку, утратою навичок, депігментацією шкіри, волосся і райдужних оболонок, судомами невстановленого характеру, що виникли в перші 6 місяців. Діагноз ФКУ встановлювався з врахуванням клінічних, параклінічних і генетичних аспектів.
Клінічно для дітей із ФКУ характерні були наступні симптоми: гіпотонія, гіперрефлексія, рухове розгальмування, зміни запаху шкіри і сечі, депігментація шкіри, волосся і райдужних оболонок, явища дерматиту, утрата навичок, судомний синдром, розумова відсталість, мікроцефалія, гіпертензійно-лікворний синдром.
При генеалогічному аналізі підтверджувався аутосомно-рецесивний характер успадкування ФКУ з генетичним ризиком 25%.
Дослідження у дітей вмісту фенілаланіну (ФА) в крові підтверджувало патологію обміну фенілаланіну. Ми виділяли групу дітей з класичною ФКУ (середній рівень ФА крові 1448,16+/-151,23 мкМ/л) і атиповою ФКУ (середній рівень ФА крові 466,12+/-39,31 мкМ/л).
В даний час на дієтотерапії гідролізатами білка і диспансерному обліці стоять діти з групи з класичною ФКУ.
Усім дітям з моменту діагностики ФКУ була розпочата дієтотерапія, побудована за принципом різкого обмеження кількості ФА, що надходить з їжею. З раціону хворих виключалися високобілкові продукти (м’ясо, риба, печінка, сир, яйця, хлібо-булочні вироби, крупи, квасоля, горох та інші).
Вікові потреби в білку (а точніше в амінокислотах) заповнювалися шляхом включення в раціон гідролізатів казеїну або сумішей амінокислот.
У наших випадках пізно діагностованої ФКУ, перед введенням гідролізату білка, проводилася 2-тижнева розвантажувальна дієта, при якій з харчування виключали молоко, м’ясо, печінку, хлібо-булочні вироби і т.п. Введення гідролізату білка починали з 1/2 дози добової потреби, поступово підвищуючи дозу в суміші з овочевими соками, частіше з томатним (для поліпшення органолептичних властивостей) у вигляді другого сніданку і полуденка.
Дієта доповнювалася введенням крахмалопродуктів (саго, сагова крупа, вермішель, кекс і хліб) виробництва Кореневського експериментального заводу крахмалопродуктів.
Дієтотерапія проводилася під щомісячним контролем ваги, росту і з щоквартальним контролем протеінограми. Контроль рівня ФА крові проводився щотижня перші три місяці дієтотерапії, при зниженні рівня ФА крові до меж 180-480 мкМ/л контроль рівня ФА крові проводився щомісяця. На 3-4 році дієтотерапії при стабільних показниках ФА крові контроль рівня ФА крові проводиться щокварталу.
Під впливом дієтотерапії в першу чергу зникав неприємний запах шкіри і сечі, нормалізувався сон, підсилювалася пігментація волосся і райдужних оболонок.
Протягом 3-5 тижнів дієтотерапії судоми більше не повторювалися. У перші 6 місяців дієтотерапії спостерігалася позитивна динаміка моторного розвитку. Ступінь інтелектуального розвитку мала чітку залежність від часу діагностики ФКУ і старанності дотримання дієти. Так, один з дітей, у якого ФКУ була діагностована в доклінічному періоді, внаслідок порушення дієтотерапії у віці 1-1,5 роки дав клінічні прояви класичної ФКУ, утратив придбані навички і, незважаючи на проведену згодом дієтотерапію, має в даний час легку розумову відсталість і навчається в спецшколі.
Порушення мови нормалізувалися значно повільніше, ніж моторні навички.
В протеінограмі дітей з ФКУ на тлі дієтотерапії спостерігалася тенденція до гіпопротеінемії.
На ехоенцефалограмі (ЕХОЕГ) відзначалося зменшення гіпертензійно-лікворного синдрому, або його зникнення.
На електроенцефалограмі (ЕЕГ) на тлі загальної гіперсинхронізації і помірних загальномозкових змін реєструвалася іритація кори з залученням серединних або стовбурових структур. Відзначалося зниження реактивності кори.
З 18 дітей, що знаходяться в даний час на дієтотерапії, значне поліпшення інтелектуального розвитку спостерігається у 10 дітей, 6 з них займаються в загальноосвітній школі по загальній програмі, із програмою справляються, але слід відзначити труднощі при вивченні математики й успіхи при вивченні мов.
4 дітей займаються в загальноосвітній школі по індивідуальній програмі. Дитина, у якої ФКУ була діагностована в доклінічному періоді і мали місце порушення дієтотерапії, навчається в спецшколі.
Велике значення в соціальній адаптації дітей з пізно виявленою ФКУ має реабілітаційна гіпотензивна і психостимулююча терапія, проведена за участю невропатолога, під контролем ЕХОЕГ і ЕЕГ щорічно.
Діти дошкільного віку отримували допомогу з соціальної адаптації в логопедичному дитячому садку. У зв’язку з відсутністю в багатьох районах області спеціалізованих дитячих садків, великих успіхів у соціальній адаптації домоглися родини, що проживають у м. Одесі.
Дієтотерапія залишається найважливішою ланкою в ланцюзі реабілітаційних заходів дітей, що страждають на ФКУ.
Одеський ММГЦ має досвід роботи з наступними гідролізатами білка: “Берлофен”, “Нофелан”, “PKU-80”, “Лофеналак”, “Тетрафен”, “Феніл-Фрі” і сумішшю амінокислот “РАМ”.
У зв’язку з економічними труднощами, забезпеченість гідролізатами білка носила нестабільний характер. Тільки останні півтора року діти, що страждають на ФКУ 100% забезпечені гідролізатом білка “Тетрафен”. Даний гідролізат добре засвоюється при поділі добової дози на 3-4 прийоми. Відмінні результати спостерігалися при дієтотерапії сумішшю амінокислот “РАМ”, єдиним недоліком є її висока ціна. Однак, з огляду на те, що половина хворих на ФКУ є дівчатками, які ще повинні стати матерями, вважаю за доцільне проводити дієтотерапію ФКУ у дівчат протягом часу, довшого за 15 років.
Залишається актуальним питання забезпечення хворих на ФКУ крахмалопродуктами.
Приклад схеми дієтотерапії фенілкетонурії, яка дозволяє утримувати рівень фенілаланіну крові в межах 2,5-4 мг%, що навіть при пізній діагностиці ФКУ дозволяє домогтися успіхів у соціальній адаптації дитини.
мг |
заг. |
гідролізату |
||||
|---|---|---|---|---|---|---|
Номер з каталогу МІМ:
261600 Phenylketonuria; PKU.
Переглянуто редакційною колегією I.B.I.S.: 05/02/2002
Дивіться також:
- Продукти з низьким вмістом фенілаланіну
- Низькобілкові продукти харчування (ФКУ) виробництва Польщі
- Кулінарні рецепти для осіб з низькофенілаланіновою дієтою
- Досвід діагностики та лікування хворих на фенілкетонурію, виявлених по програмі скринінгу
- Фенілкетонурія (інформація для спеціалістів)
- Фенілкетонурія (інформація для батьків)
Фенілкетонурія
(Phenylketonuria, PKU)
Сергій Лапченко
Інформаційний спеціаліст Волинського ОМНІ-центру
Фенілкетонурія – це спадкове захворювання, яке, за умови відсутності лікування, призводить до розумової відсталості. Хоча ця хвороба не дуже поширена (1 дитина з кожних 8000 новонароджених), вона потребує великих витрат. В США, наприклад, щороку витрачається кілька мільйонів доларів на лікування хворих дітей. Але навіть це не можна порівняти з тим горем, яке приходить в сім’ю з народженням хворої дитини.
Що таке фенілкетонурія?
Фенілкетонурія – це хвороба, яка змінює метаболізм (здатність організму засвоювати їжу). Діти, народжені з фенілкетонурією, не здатні метаболізувати фенілаланін (частина протеїну), який через це накопичується в крові. Така ненормальна висока кількість фенілаланіну перешкоджає нормальному розвитку мозку.
Як все це впливає на дитину?
Діти, які народилися з фенілкетонурією, в перші кілька місяців життя здаються цілком нормальними. Але якщо лікування не розпочато, через 3-5 місяців вони починають втрачати інтерес до оточення, коли їм виповнюється рік, вони вже є розумово відсталі. Діти з фенілкетонурією часто є дратівливі, неспокійні і невгамовні. Навколо них можна почути запах плісняви, вони часто мають суху шкіру і висипку на ній. Деякі навіть можуть мати конвульсії (судоми). Як правило, вони дуже добре розвиваються фізично і мають світліше волосся ніж їх родичі.
Яким чином передається ця хвороба?
Фенілкетонурія є спадковою хворобою, вона проявляється лише тоді, коли обидва батьки мають ген хвороби і передають його дитині. Якщо в кожній клітині є один нормальний ген і один ген фенілкетонурії,- то така людина називається носієм. Вона не має ніяких проявів хвороби, але може передати хворобливий ген своїм нащадкам.
Якщо обидва батьки є носіями, то існує 25% шансів (1 із 4), що кожен з них передасть дефектний ген дитині, викликаючи таким чином народження хворої дитини (див. діаграму). Є також 25% шансів (1 із 4), що вони передадуть здорові гени і дитина народиться цілком здоровою. І, нарешті, є 50% шансів (2 із 4), що у дитини буде один нормальний ген і один ген фенілкетонурії. В цьому випадку дитина буде носієм, як і її батьки.
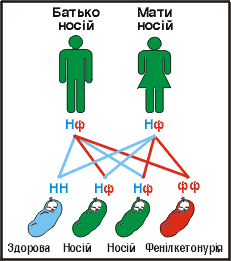 Для кожної вагітності шанси однакові, тому в сім’ї всі діти можуть бути як здоровими, так і хворими на фенілкетонурію, або бути носіями.
Для кожної вагітності шанси однакові, тому в сім’ї всі діти можуть бути як здоровими, так і хворими на фенілкетонурію, або бути носіями.
Чи є можливість діагностувати фенілкетонурію?
Так. За допомогою спеціального тестування крові (потрібно лише кілька крапель) можливо діагностувати хворобу, коли дитина має лише 2 дні і знаходиться в пологовому будинку. Проби крові аналізуються на вміст фенілаланіну і визначається причина його підвищення, якщо таке є.
Існує також тест сечі, але він дає менш надійні результати.
Чи можливо лікувати фенілкетонурію?
Так. Дитина переводиться на спеціальну дієту з низьким вмістом фенілаланіну. Це означає повну неприйнятність коров’ячого молока, звичайних молочних сумішей або м’яса, бо ці продукти мають забагато фенілаланіну.
Спочатку дитину годують тільки спеціальною молочною сумішшю, в якій зовсім немає фенілаланіну. Пізніше додають певні овочі та інші продукти з низьким вмістом цього виду протеїну.
Дитина з фенілкетонурією потребує регулярного тестування крові, тому що харчування залежить від вмісту фенілаланіну в ній. Ніхто не знає, як довго повинна залишатись дитина на подібній дієті. Є дані, що припинення дієтичного харчування у віці 6-8 років може привести до змін у поведінці та розвитку нездатності до навчання. Всі ці питання батьки повинні вирішувати тільки з лікарями, які пройшли спеціальну підготовку з фенілкетонурії.
Чи може хвора на фенілкетонурію жінка мати дітей?
Коли жінка з фенілкетонурією стає вагітною, скоріше за все її дитина народиться розумово відсталою. Сьогодні це стало величезною проблемою, бо, якщо ці жінки притримувалися лікування, вони виросли цілком нормальними і тепер мають власних дітей. Їх діти рідко успадковують фенілкетонурію, але їх мозок ще в утробі пошкоджений ненормальним метаболізмом матері. Звичайно, таким дітям дієта допомогти вже не може.
Одначе, розумовій відсталості можна запобігти, якщо мати відновить дієту до початку і під час вагітності. Проблема в тому, що жінки часто вагітніють, не бажаючи цього, і ушкодження мозку плода може початись до того, як дієтичне харчування стане ефективним. Крім того, така дієта дорого коштує, незручна і неприємна для людей, які вже звикли до нормальної їжі. Часом жінки забувають, що вони в дитинстві колись їли спеціальну їжу, або їм цього не розповідають батьки.
Можливо, з часом з’являться ефективніші методи лікування і запобігання фенілкетонурії, вчені працюють над цими питаннями, в той час як лікарі постійно намагаються впроваджувати нові досягнення в практику охорони здоров’я.
Переглянуто редакційною колегією I.B.I.S.: 05/02/2002
Дивіться також:
- Продукти з низьким вмістом фенілаланіну
- Низькобілкові продукти харчування (ФКУ) виробництва Польщі
- Кулінарні рецепти для осіб з низькофенілаланіновою дієтою
- Досвід діагностики та лікування хворих на фенілкетонурію, виявлених по програмі скринінгу
- З досвіду лікування фенілкетонурії при пізній діагностиці в Одеському ММГЦ
- Фенілкетонурія (інформація для спеціалістів)
Кулінарні рецепти для осіб на низькофенілаланіновій дієті
(Low Phenylalanine Diet Cooking Recipes)
Наталія Афанасьєва
кандидат медичних наук
завідуюча Кримським республіканським медико-генетичним центром
Зінаїда Живац
кандидат медичних наук
завідуюча Одеським міжобласним медико-генетичним центром
Низькобілкова ковбаса
Склад і спосіб приготування ковбасної маси для наведених нижче ковбасних рецептів:
- 500 г шкурки від сала (гомілка ніжки);
- 900 г сала;
- 150 г низькобілкової муки;
- 90 г цибулі;
- 80 г моркви;
- 80 г селери;
- сіль, перець, зелень.
Приготування:
Шкірку, сало і цибулю порізати шматочками, відварити до м’якого стану в невеликій кількості воді. Відділити бульйон від приготованих продуктів для приготування інших видів низькобілкової ковбаси. 250 г відвареного сала відложити для приготування “кров’янки”. Відварені продукти перемішати до отримання однорідної маси.
Ковбаса для смаження
- 600 г ковбасної маси (300,0 мг ФА; 7,9 г білка);
- 30 г ковбасної маси (15,0 мг ФА; 0,4 г білка).
Продукти:
- 200 г відвареного сала, перетертого на пюре (180,0 мг ФА; 4,6 г білка);
- 100 г відвареної шкурки від сала, перетертої на пюре (90,0 мг ФА; 2,3 г білка);
- 35 г тушкованої цибулі, перетертої на пюре (100 г сирої) – (25,0 мг ФА; 0,9 г білка);
- 100 г смальцю (5,0 мг ФА; 0,1 г білка);
- 165 г бульйону;
- Сіль, перець, зелень.
Всього: 300,0 мг ФА; 7,9 г білка
Приготування:
Всі компоненти добре перемішати і додати приправу згідно смаку. Наповнити отриманою масою тонкі кишки. Випікати 45 хвилин при температурі 80 градусів або стерилізувати в скороварці.
Ковбаса для смаження ІІ
- 600 г ковбасної маси (200,0 мг ФА; 5,5 г білка);
- 30 г ковбасної маси (10,0 мг ФА; 0,3 г білка).
Продукти:
- 100 г відвареного сала, перетертого на пюре (90,0 мг ФА; 2,3 г білка);
- 50 г відвареної шкурки від сала, перетертої на пюре (45,0 мг ФА; 1,2 г білка);
- 50 г тушкованої цибулі (30,0 мг ФА; 1,4 г білка);
- 100 г смальцю (5,0 мг ФА; 0,1 г білка);
- 90 г низькобілкового хліба (22,0 мг ФА; 0,5 г білка);
- 210 мл бульйону;
- Сіль, перець, зелень.
Всього: 200,0 мг ФА; 5,5 г білка
Приготування:
Сушений хліб розмочити в бульйоні, додати до маси інші компоненти, приправи, наповнити тонкі кишки. Випікати в духовці чи скороварці.
Ковбаса з овочами
- 600 г ковбасної маси (300,0 мг ФА; 8,0 г білка);
- 330 г ковбасної маси (15,0 мг ФА; 0,4 г білка).
Продукти:
- 90 г цибулі-порей (69,0 мг ФА; 1,7 г білка);
- 80 г картоплі (25,0 мг ФА; 0,8 г білка);
- 80 г селери (51,0 мг ФА; 1,3 г білка);
- 80 г цибулі (20,0 мг ФА; 0,7 г білка);
- 120 мл бульйону;
- 100 г відвареного сала (пюре) – (90,0 мг ФА; 2,3 г білка);
- 50 г відвареної шкурки від сала (пюре) – (45,0 мг ФА; 1,2 г білка);
- Сіль, перець, зелень.
Всього: 300,0 мг ФА; 8,0 г білка
Приготування:
Овочі порізати, потушкувати в бульйоні. Подрібнити, перемішати з ковбасною масою, додати спеції, наповнити тонкі кишки. Випікати в духовці чи скороварці.
Кров’янка домашня
- 500 г ковбасної маси (170,0 мг ФА; 4,6 г білка);
- 30 г ковбасної маси (10,0 мг ФА; 0,3 г білка).
Продукти:
- 100 г відвареного сала (90,0 мг ФА; 2,3 г білка);
- 50 г відвареної шкурки від сала (45,0 мг ФА; 1,2 г білка);
- 30 г цибулі (90 г сирої) – (22,0 мг ФА; 0,8 г білка);
- 150 мл бульйону;
- 50 мл крові свинячої (13,0 мг ФА; 0,3 г білка);
- 120 г хліба низькобілкового;
- 1 чайна ложка солі, перцю;
- 1/2 чайної ложки майоранку;
- Щіпка петрушки, гвоздики тертої.
Всього: 170,0 мг ФА; 4,6 г білка
Приготування:
Сушений хліб розмочити в бульйоні, перемішати з іншими компонентами. Отриманою масою наповнити тонкі кишки. Випікати.
Овочеве блюдо
- 90,0 мг ФА;
- 3,2 г білка.
Продукти:
- 100 г огірків (13,0 мг ФА; 0,6 г білка);
- 80 г помідорів (13,0 мг ФА; 0,7 г білка);
- 65 г моркви (20,0 мг ФА; 0,7 г білка);
- 30 г печериць (консервованих) – (19,0 мг ФА; 0,7 г білка);
- 20 г сметани 30% (24,0 мг ФА; 0,5 г білка);
- 2 г петрушки;
- 10 г соняшникової олії;
- Кріп, базилік, сіль, бульйон, перець горошком.
Всього: 90,0 мг ФА; 3,2 г білка
Приготування:
З помідора зрізати шкірку, почистити огірки, моркву. Все порізати на шматочки, потушкувати в маслі. Додати зелень, трохи води. Тушкувати з закритою кришкою на маленькому вогні 15 хвилин. В кінці додати сметани та дрібно порізаних печериць, петрушки. На гарнір: відварені низькобілкові макарони.
Пікантні налисники з цибулею
- 15,0 мг ФА;
- 0,6 г білка.
Продукти:
- 100 г низькобілкового борошна (5,0 мг ФА; 0,3 г білка);
- 1 чайна ложка порошку для печива;
- 1 чайна ложка соняшникової олії;
- 100 мл води (в т.ч. 50 мл мінеральної води);
- Сіль згідно смаку;
- 30 г тушкованої цибулі (8,0 мг ФА; 0,3 г білка).
Всього: 13,0 мг ФА; 0,6 г білка
Приготування:
З усіх компонентів вимішати тісто, перемішати з цибулею, випікати на сковорідці в гарячій олії.
Печені шарики
- 400,0 мг ФА;
- 0,6 г білка.
Продукти:
- 250 г картопляного пюре (207,0 мг ФА; 4,8 г білка);
- 240 г пюре з гарбуза (58,0 мг ФА; 1,4 г білка);
- 160 г подрібненої відвареної зеленої квасолі (стручкової) – (37,0 мг ФА; 1,2 г білка);
- 125 г тушкованої цибулі (6,0 мг ФА; 0,1 г білка);
- 40 г картопляного крохмалю;
- 40 мл води;
- 120 г свіжої моркви, подрібненої міксером (31,0 мг ФА; 1,1 г білка);
- Щіпка перемішаної зелені;
- Сіль, перець.
Всього: 400,0 мг ФА; 10,1 г білка
Приготування:
Розчинити крохмаль в холодній воді. Перемішати всі компоненти, влити розчинений крохмаль. На маленькому вогні довести до густого стану. З охолодженої маси зліпити шарики та обсмажити в сухарях низькобілкової булки чи в борошні.
Гамбургер (булка низькобілкова)
- 150,0 мг ФА;
- 3,8 г білка.
Продукти:
- 18 г дріжджів (62,0 мг ФА; 1,4 г білка);
- 80 г мінеральної газованої води кімнатної температури;
- 100 г низькобілкового борошна (5,0 мг ФА; 0,3 г білка);
- 10-15 г рослинної олії;
- Сіль.
Всього: 67,0 мг ФА; 1,7 г білка
Приготування:
Дріжжі розчинити в теплій воді, додати борошно, рослинну олію, сіль і замісити тісто. Якщо тісто буде рідким, додати ще трохи борошна. З тіста зробити дві булки, залишити на 20 хвилин, щоб тісто піднялося, і випікати. Після випічки змастити теплою водою.
Начинка до гамбургера
- 83,0 мг ФА;
- 2,1 г білка.
Продукти:
- 50 г картопляного пюре (45,0 мг ФА; 1,0 г білка);
- 50 г пюре з гарбуза (12,0 мг ФА; 0,3 г білка);
- 40 г зеленої стручкової квасолі (12,0 мг ФА; 0,3 г білка);
- 30 г подрібненої свіжої моркви (6,0 мг ФА; 0,2 г білка);
- 30 г тушкованої цибулі (8,0 мг ФА; 0,3 г білка);
- 10-15 г картопляного крохмалю;
- Суміш сушених приправ: майоранк, розмарин, тим’ян, петрушка, сіль, перець.
Всього: 83,0 мг ФА; 2,1 г білка
Приготування:
Картопляне пюре, овочеве пюре і приправи помістити в каструлю та додати розчинений у воді картопляний крохмаль. Далі на маленькому вогні, перемішуючи, готувати до загустіння. Масу охолодити. Зліпити два гамбургери. Обкласти ними низькобілкову булку і підсмажити в гарячій олії.
Смажені овочеві оладки
- 140,0 мг ФА;
- 3,4 г білка.
Продукти:
- 125 г картоплі (113,0 мг ФА; 2,6 г білка);
- 50 г моркви (16,0 мг ФА; 0,5 г білка);
- 35 г цибулі (9,0 мг ФА; 0,3 г білка);
- 20 г низькобілкового борошна (2,0 мг ФА);
- Сіль, перець, майоранк.
Всього: 140,0 мг ФА; 3,4 г білка
Приготування:
Перетерти на тертці сирими картоплю, моркву, цибулю. Додати борошно, приправи і перемішати. З тіста випекти оладки в гарячому маслі.
Цибуля-порей в тісті
- 100,0 мг ФА;
- 2,5 г білка.
Продукти:
- 100 г цибулі-порей (76,0 мг ФА; 1,9 г білка);
На тісто:
- 1 столова ложка сметани (18,0 мг ФА; 0,4 г білка);
- 2 столових ложки низькобілкового борошна (2,0 мг ФА; 0,1 г білка);
- Вода, сіль, перець.
Всього: 96,0 мг ФА; 2,4 г білка
Приготування:
Стебло цибулі-порей помістити в окріп на 10-15 хвилин. З сметани, води, борошна і приправ замісити тверде тісто. Порей порізати на шматки довжиною 5 см. Тісто тонко розкачати і загорнути кожний шматок порея окремо. Обваляти в сухарях та засмажити в гарячій олії.
Піцца
- 150,0 мг ФА;
- 5,2 г білка.
Продукти:
- 8 г свіжих дріжджів (62,0 мг ФА; 1,3 г білка);
- 100 мл мінеральної води кімнатної температури;
- 120 г низькобілкової муки (6,0 мг ФА; 0,4 г білка);
- 1 столова ложка маслинової олії;
- Сіль згідно смаку.
Начинка:
- 120 г помідорів (19,0 мг ФА; 0,1 г білка);
- 50 г печериць (31,0 мг ФА; 1,4 г білка);
- 50 г цибулі (13,0 мг ФА; 0,5 г білка);
- 20 г сала (18,0 мг ФА; 0,5 г білка);
- 1 столова ложка олії (маслинової чи соняшникової);
- Сіль, перець, приправи.
Всього: 149,0 мг ФА; 5,2 г білка
Приготування:
Тісто: дріжджі розчинити в невеликій кількості води. Вимішати з борошном, олією і сіллю. Тонко викласти тісто в невелику форму для тортів. Залишити на 20 хвилин. Потім викласти на тісто компоненти для начинки. Приправити і полити олією. Випікати в духовці 15-20 хвилин.
Фарширований болгарський перець
- 100,0 мг ФА;
- 2,5 г білка.
Продукти:
- 100 г перцю болгарського (36,0 мг ФА; 0,9 г білка);
Начинка:
- 50 г низькобілкового хліба (черствого) – (13,0 мг ФА; 0,3 г білка);
- 20 г сметани 30% (24,0 мг ФА; 0,5 г білка);
- 20 г цибулі (5,0 мг ФА; 0,2 г білка);
- Вода;
- Щіпка петрушки.
Соус:
- 20 г рослинної олії;
- 25 г томатного соусу (тертого помідора) – (23,0 мг ФА; 0,6 г білка);
- 100 мл води;
- 1 столова ложка кукурудзяного борошна;
- Сіль, перець, тим’ян, цукор.
Всього: 100,0 мг ФА; 2,5 г білка
Приготування:
З перця зрізати кришечку, витягнути зерна. Залити окропом, витримати 10 хвилин. Дрібно порізати хліб, залити сметаною, розмішаною в малій кількості води. Подрібнену цибулю потушкувати в маргарині, перемішати з хлібом. Додати приправи. Наповнити масою перець. Викласти в каструлю. Приготувати соус. Залити фаршировані перці. Тушкувати з закритою кришкою 15-20 хвилин.
Голубці з капусти
- 200,0 мг ФА;
- 4,9 г білка.
Продукти:
- 110 г білої капусти (84,0 мг ФА; 2,0 г білка);
- 50 г картоплі (15,0 мг ФА; 0,5 г білка);
- 15 г жирного свиного фаршу (65,0 мг ФА; 1,4 г білка);
- 20 г цибулі (5,0 мг ФА; 0,2 г білка);
- 100 г низькобілкового хліба (30,0 мг ФА; 0,8 г білка);
- Сіль, перець.
Всього: 200,0 мг ФА; 4,9 г білка
Приготування:
Хліб замочити в невеликій кількості води, перетерти разом з відвареною морквою. Дрібно порізану цибулю перемішати з м’ясним фаршем, приправити. Перемішати всі компоненти. Листя капусти відварити в солоній воді. Викласти начинку. Загорнути кожен лист в “конвертик”. Обсмажити кожен голубець з обох боків в гарячій олії.
Баклажани (кабачки) фаршировані
- 101,0 мг ФА;
- 3,5 г білка.
Продукти:
- 150 г баклажанів (42,0 мг ФА; 1,1 г білка).
Начинка:
- 1-2 столової ложки рослинної олії;
- 100 г цибулі (26,0 мг ФА; 0,9 г білка);
- 150 г помідорів (29,0 мг ФА; 1,4 г білка);
- 1/2 зубчика часнику;
- 2 г петрушки (4,0 мг ФА; 0,1 г білка);
- Щіпка солі, цукру, 1/4 лаврового листя.
Всього: 101,0 мг ФА; 3,5 г білка
Приготування:
Баклажан розрізати на дві половини. Видалити з них м’якуш. Половинки обсмажити в олії. Притушкувати в олії цибулю, кусочки помідорів без шкірки, дрібно порізаний м’якуш баклажана. В кінці додати дрібно порізаний часник, приправи, зелень. Половинки обсмажених баклажанів наповнити приготованою масою. Покласти зверху шматки помідорів, трошки посолити. Випікати в духовці 15 хвилин.
Вафлі на дріжджах
- 100,0 мг ФА;
- 2,7 г білка.
Продукти:
- Біля 200 мл води;
- 5 г дріжджів (39,0 мг ФА; 0,8 г білка);
- 125 г низькобілкового борошна (6,0 мг ФА; 0,4 г білка);
- 25 мл сметани (30,0 мг ФА; 0,6 г білка);
- Щіпка солі;
- 1 чайна ложка ванільного цукру;
- 100 г чорниць з цукром (26,0 мг ФА; 0,9 г білка).
Всього: 100,0 мг ФА; 2,7 г білка
Приготування:
Дріжджі розчинити в теплій воді, потім домішати компоненти для тіста. Тісто залишити в посуді на 5-10 хвилин. Потім випекти вафельки в вафельниці. Посипати пудрою. Подавати з ягодами.
Тісто кокосове
- 160,0 мг ФА;
- 3,6 г білка.
Продукти:
- 125 г маргарину рослинного;
- 100 г цукру;
- 1 пачка ванільного цукру;
- 120 мл мінеральної води з температурою 20°;
- 50 г кокосової стружки (145,0 мг ФА; 2,8 г білка);
- 250 г низькобілкового борошна (13,0 мг ФА; 0,8 г білка;
- 1 чайна ложка порошку для печива.
Всього: 160,0 мг ФА; 3,6 г білка
Приготування:
Маргарин, цукор, ванільний цукор збити до пухкої маси. Борошно перемішати з порошком для печива, з кокосовою стружкою. З’єднати обидві частини. Тісто помістити в невелику форму для тортів і випікати приблизно 30 хвилин.
Торт з яблуками
- 15,0 мг ФА;
- 0,7 г білка.
Продукти:
- 100 г низькобілкового борошна (5,0 мг ФА; 0,3 г білка);
- 1 столова ложка цукру;
- 1 чайна ложка рому чи коньяку;
- 50 г рослинного маргарину;
- 90 г яблук (6,0 мг ФА; 0,2 г білка);
- Трохи кориці.
Присипка:
- 50 г низькобілкового борошна (3,0 мг ФА; 0,2 г білка);
- 1 чайна ложка цукру;
- 1/2 чайної ложки ванільного цукру;
- 25 г рослинного маргарину.
Всього: 15,0 мг ФА; 0,7 г білка
Приготування:
З борошна, цукру, рому чи коньяку та маргарину замісити тісто і помістити в невелику форму для тортів. Яблука порізати на півкружечки і викласти на тісто. Посипати корицею. З компонентів, що залишились, розтерти присипку і посипати яблука. Випікати 30-40 хвилин.
Рецепт тіста дріжджового
- 68,0 мг ФА;
- 1,4 г білка.
Продукти:
- 8 г свіжих дріжджів (62,0 мг ФА; 1,3 г білка);
- 80 мл мінеральної води з температурою 20°;
- 120 г низькобілкового борошна (6,0 мг ФА; 0,1 г білка);
- 1 столова ложка рослинної олії (маслинової чи соняшникової);
- Сіль згідно смаку.
Всього: 68,0 мг ФА; 1,4 г білка
Приготування:
Дріжджі розчинити в невеликій кількості теплої води. Перемішати з борошном, рослинною олією, сіллю. Помістити у форму для випікання і залишити на 15-20 хвилин. Випікати в духовці 40-45 хвилин.
Переглянуто редакційною колегією I.B.I.S.: 05/02/2002
Дивіться також:
- Продукти з низьким вмістом фенілаланіну
- Низькобілкові продукти харчування (ФКУ) виробництва Польщі
- З досвіду лікування фенілкетонурії при пізній діагностиці в Одеському ММГЦ
- Досвід діагностики та лікування хворих на фенілкетонурію, виявлених по програмі скринінгу
- Фенілкетонурія (інформація для спеціалістів)
- Фенілкетонурія (інформація для батьків)
Продукти з низьким вмістом фенілаланіну
(Low Phenylalanine-Containing Foods)
Наталія Афанасьєва
кандидат медичних наук
завідуюча Кримським республіканським медико-генетичним центром
Зінаїда Живац
кандидат медичних наук
завідуюча Одеським міжобласним медико-генетичним центром
Для полегшення підрахунку фенілаланіну (ФА) в продуктах харчування для дітей нижче наведена інформація про вміст в них фенілаланіну, білків, жирів та вуглеводів.
Соки
Хлібо-булочні вироби, борошно, бульйон, приправи
(вміст в 100 г)
(ккал) |
(г) |
(г) |
(г) |
||
|---|---|---|---|---|---|
Овочі (вміст в 100 г)
(мг) |
(ккал) |
(г) |
(г) |
(г) |
(мг) |
|||
|---|---|---|---|---|---|---|---|---|
довж. 20 |
||||||||
стручків |
||||||||
консервований |
||||||||
суцвіття |
||||||||
шаткованої |
||||||||
шаткованої |
||||||||
ложка |
||||||||
ложка |
||||||||
довж. 12 см |
||||||||
1 малий |
13 |
50 |
||||||
довж. 14 см |
||||||||
довж. 14 см |
||||||||
1 малий |
37 |
37 |
||||||
1 малий |
12 |
50 |
||||||
1 вел. лист 1 вел. пучок |
10 228 |
10 250 |
||||||
приготування |
||||||||
ложка |
Фрукти, ягоди (вміст в 100 г)
(мг) |
(ккал) |
(г) |
(г) |
(г) |
(мг) |
|||
|---|---|---|---|---|---|---|---|---|
середнього |
||||||||
1 малий |
18 |
50 |
||||||
1 велике |
17 |
140 |
||||||
1 великий |
20 |
80 |
||||||
1/2 стакана |
110 |
130 |
||||||
10 середніх |
29 |
160 |
||||||
8 великих |
24 |
100 |
||||||
гроно |
||||||||
ложка |
||||||||
Жири (вміст в 100 г)
(мг) |
(ккал) |
(г) |
(г) |
(г) |
(мг) |
|||
|---|---|---|---|---|---|---|---|---|
чайна ложка |
||||||||
чайна ложка |
||||||||
чайна ложка |
||||||||
чайна ложка |
||||||||
чайна ложка |
||||||||
чайна ложка |
||||||||
чайна ложка |
||||||||
чайна ложка |
||||||||
чайна ложка |
||||||||
чайна ложка |
||||||||
1 ст. ложка |
0 |
12 |
||||||
1 ст. ложка |
0 |
12 |
||||||
1 ст. ложка |
0 |
12 |
||||||
1 ст. ложка |
0 |
12 |
||||||
1 ст. ложка |
0 |
12 |
||||||
1 ст. ложка |
0 |
12 |
||||||
1 стакан |
250 |
250 |
||||||
1 стакан |
285 |
250 |
||||||
1 стакан |
298 |
250 |
||||||
1 стакан |
320 |
250 |
Цукор, мед та солодкі вироби
(вміст в 100 г)
(мг) |
(ккал) |
(г) |
(г) |
(г) |
(мг) |
|||
|---|---|---|---|---|---|---|---|---|
без верху 1 ч. ложка з верхом 1 ст. ложка без верху |
0 0 |
10 15 |
||||||
1 ст. ложка |
0 |
30 |
||||||
без верху |
||||||||
без верху |
||||||||
без верху |
||||||||
без верху |
||||||||
без верху |
||||||||
без верху |
||||||||
без верху |
||||||||
без верху |
||||||||
без верху |
||||||||
без верху |
||||||||
без верху |
||||||||
без верху |
||||||||
без верху |
||||||||
без верху |
||||||||
Переглянуто редакційною колегією I.B.I.S.: 05/02/2002
Дивіться також:
- Низькобілкові продукти харчування (ФКУ) виробництва Польщі
- Кулінарні рецепти для осіб з низькофенілаланіновою дієтою
- З досвіду лікування фенілкетонурії при пізній діагностиці в Одеському ММГЦ
- Досвід діагностики та лікування хворих на фенілкетонурію, виявлених по програмі скринінгу
- Фенілкетонурія (інформація для спеціалістів)
- Фенілкетонурія (інформація для батьків)
Досвід діагностики та лікування хворих на фенілкетонурію, виявлених по програмі скринінгу
(Phenylketonuria Diagnosis and Treatment)
Наталія Афанасьєва
кандидат медичних наук
завідуюча Кримським республіканським медико-генетичним центром
Фенілкетонурія (ФКУ) – захворювання обміну амінокислоти фенілаланіну, при якому у хворих розвивається розумова відсталість, судомний синдром, зміни з боку шкіри з аутосомно-рецесивним типом наслідування. На Україні ця хвороба зустрічається з частотою 1 на 8000 новонароджених, в Криму 1:7375, згідно даних Київського медико-генетичного центру (МГЦ) 1:6000 новонароджених.
Хвороба вперше описана Феллінгом в 1934 році, її патогенез активно вивчався в 50-60-х роках ХХ століття. Ервісом в 1947 році було показано, що біохімічні порушення пов’язані з дефіцитом ферменту фенілаланінгідроксилази (ФАГ). В 1961 році Гатрі запропонував мікробіологічний інгібіторний тест, який дозволив широко проводити скринінг новонароджених в пологових будинках. В 1953 році Биккель розробив основний принцип терапії ФКУ – обмеження фенілаланіну (ФА) в раціоні хворих (дієтотерапія). В 70-х роках почались дослідження молекулярної основи ФКУ. В 1984 році був картований ген ФАГ на 12 хромосомі, тепер молекулярно-генетичне обстеження хворих та носіїв гену стало широко впроваджуватися в практичну охорону здоров’я.
До основних принципів лікування ФКУ відносяться:
- початок лікування до настання клінічних проявів, тобто практично з 1,5-2 місяців життя дитини;
- дієта з низьким вмістом протеіну та з вживанням спеціальних сумішей (замінників білка) без ФА;
- постійна корекція дієтотерапії під контролем визначення ФА в сироватці крові;
- постійне дотримання дієти до закінчення пубертатного періоду.
Розглянемо детальніше ці принципи:
1. Ранній початок терапії означає проведення скринінгової програми в пологових будинках. Без чітко налагодженого скринінгу отримати добрих результатів в лікуванні ФКУ неможливо. Автономна Республіка Крим відноситься, напевно, до небагатьох регіонів України, де програма скринінгу новонароджених на виявлення ФКУ з 1989 року не припинялася ні на один день. Досвід проведення скринінгу показує, що хоча його правила і є добре відомі і закріплені наказом № 77 МОЗ України, існує ряд ключових моментів, на які потрібно звернути особливу увагу.
По-перше, дуже важливо контролювати час забору крові, в іншому випадку можливі псевдонегативні результати. В нашій практиці був такий випадок: до медико-генетичного центру (МГЦ) звернулась сім’я з дитиною 8 місяців життя зі скаргами на затримку психомоторного розвитку. При обслідуванні був виявлений рівень ФА крові 20 мг%. Виявилось, що дитина була обстежена за скринінг-програмою і в зразку крові, отриманому з пологового будинку, ФА не перевищував 2 мг% (дані аналізу були ретроспективно перевірені в Криворізькому медико-генетичному центрі). В цьому випадку причиною низького рівня ФА у хворого на ФКУ в пологовому будинку став забір крові на 1-2 день життя, коли дитина ще не отримала достатньої кількості грудного молока. В літературі також зустрічаються описи випадків псевдонегативних результатів; більшість авторів вважають, що поодинокі випадки пропуску ФКУ при скринінгу можливі саме за рахунок технічних помилок під час забору крові. Тому на бланку із зразком крові обов’язково повинні стояти дві дати: пологів та забору крові.
Інший необхідний момент при проведенні скринуючої програми – це її максимальне охоплення. З 1992 року ми розпочали облік забору крові у новонароджених в пологових будинках по прізвищах. При відсутності зразка крові дитини, її забір здійснюється за місцем проживання чи у відділеннях стаціонарів для новонароджених, якщо дитина переводиться туди до 4-го дня життя. Такий облік новонароджених дозволяє прослідкувати за кожною дитиною, що забезпечує охоплення скринінгом до 98-99% дітей.
Дуже важливим виявляється і час, що його займає верифікація діагнозу. При позитивному тесті сім’я викликається в Кримський МГЦ для повторного тестування і уточнення діагнозу. Все це повинно бути зроблене до 1,5-2 місяців життя, в протилежному випадку програма втрачає сенс. Для прискорення процесу виклику сім’ї ми використовуємо телефонограми в поліклініку за місцем проживання сім’ї і письмові повідомлення на домашню адресу батьків.
Своєрідним контролем якості проведення масового скринінгу новонароджених є пізнє виявлення хворих на ФКУ. В Криму випадків пізнього виявлення з 1993 року не було.
2. Призначення дієти. Найскладнішим моментом є первинний прийом сім’ї із нововиявленою хворою дитиною. Дуже важливо встановити контакт з батьками, добитися того, щоб вони повірили лікарю і стали неухильно дотримуватись усіх його рекомендацій. Переконати мати відлучити дитину від груді і почати дозоване годування спеціальними сумішами буває дуже важко. Тому з метою адаптації і матері і дитини ми радимо госпіталізувати дітей із підтвердженим діагнозом ФКУ у відділення патології новонароджених, де можна підібрати адекватну дієтотерапію під оперативним контролем рівня ФА сироватки крові. Останнім часом жителям навколишніх регіонів (м. Сімферополь і Сімферопольський район) при доброму контакті з сім’єю ми призначаємо дієту амбулаторно, щоб уникнути внутрішньолікарняної інфекції у відділенні для новонароджених.
Усім хворим на ФКУ призначається дієта із застосуванням білкових гідролізатів чи амінокислотних сумішей, що забезпечують концентрацію ФА сироватки крові до 4-6 мг%. Завдання лікаря навчити матір правильному розрахунку дієти. Для цього ми даємо роздруковані методичні рекомендації з розрахунку дієти з таблицями вмісту білків, жирів, вуглеводів та калорій в харчових продуктах. Незалежно від наявної суміші схема призначення дієти є загальною:
- Визначення загальної добової потреби в білку (згідно таблиць).
- Підрахунок допустимої кількості ФА на добу (згідно таблиць).
- Визначення допустимої кількості білка за рахунок натуральних продуктів.
- Визначення кількості білка за рахунок суміші.
- Розрахунок кількості суміші на добу.
- Розрахунок усього добового раціону.
Розглянемо розрахунок дієти для двомісячної дитини вагою 5 кг.
- Загальний білок на добу: 2,2 х 5 = 11 г/доб.
- ФА на добу: 60 х 5 = 300 мг/доб.
- Білок натуральних продуктів на добу: 300 : 50 = 6 г/доб.
- Білок суміші на добу: 11 – 6 = 5 г/доб.
- Кількість суміші на добу: (5 х 100) : кількість білку в 100 г сухого продукту суміші.
Різні суміші мають свій вміст білка: “PKU 1-mix” – 10,3 г, “Лофеналак” – 15 г. Якщо ваша дитини буде отримувати “Лофеналак”, то на добу їй буде потрібно біля 33 г суміші.
Стандартне розведення суміші вказане на кожній банці. Така кількість відповідає 300 г на добу.
Крім суміші дитина повинна отримати і натуральні продукти. У двомісячному віці – це грудне молоко. Молоко необхідно зціджувати і давати дозовано згідно розрахунку. В таблицях знаходимо, що в 100 г жіночого молока міститься 1,2 г білка. Ми можемо дати 6 г. Складаємо пропорцію: 1,2 г – 100 г; 6 г – х г. Х = 600 : 1,2 = 500 г молока/доб. Проводимо корекцію об’єму спожитої їжі з врахуванням кількості годувань. Непогано також провести підрахунок калорій, жирів та вуглеводів.
Якщо дитина знаходиться на штучному вигодовуванні, то натуральним продуктом для неї буде та дитяча суміш, яку вона отримує. Всі складові частини, як правило, написані на банці.
В подальшому корекція дієти здійснюється з обов’язковим визначенням рівня ФА 1 раз на тиждень до 1 року життя, а потім 1 раз на місяць до 3 років та 1 раз на квартал дітям, які старше 3 років.
З віком вводяться прикорми у звичайні терміни, але завжди з вираховуванням по таблиці вмісту в продуктах білка. При правильному розрахунку дієти із своєчасною корекцією на вік і вагу застосування будь-яких лікарських препаратів непотрібне.
При лікуванні ФКУ постійно приходиться розраховувати дієту вручну, хоча вже давно існують програми розрахунку по віку і вазі, з врахуванням натуральних продуктів та з меню – раскладкою на кожен день.
При диспансерному нагляді за хворими з ФКУ треба мати на увазі наступне: рівень ФА крові може коливатися з різних причин. Так, він підвищується при будь-яких інтеркурентних захворюваннях, іноді при прорізуванні зубов, а також через природні коливання обміну. Багато лікарських препаратів підвищують ФА, наприклад, група ноотропів, судинні засоби. Треба пам’ятати що забір крові на ФА проводиться натщесерце, інакше цифри будуть невірними.
Завжди і батьки і лікарі задають питання про щеплення: чи не є ФКУ протипоказом для щеплення? Ні, не є. Протипокази при лікованій ФКУ такі ж, як і для всіх. Єдиним зауваженням є те, що від щеплень треба утриматись, доки твердо не встановився рівень ФА крові, а також під час будь-яких порушень дієти з підвищенням ФА.
До якого віку треба притримуватись дієти? Це питання завжди вирішується індивідуально, в залежності від толерантності дитини до ФА. Однак, практика говорить, що до закінчення пубертатного віку дієти потрібно притримуватись навіть найменш ураженим дітям.
Дотримання усіх вище наведених правил гарантує здоровий інтелект у дитини. У наших хворих, які почали лікування до 2-х місяців життя, інтелект відповідає віку у 70% випадків. Затримка розвитку була в сім’ях, де батьки не дотримувались дієти, не приїздили на консультацію і контроль ФА.
Треба пам’ятати, що крім класичної ФКУ чи ФКУ1 є атипові форми, пов’язані з дефектами гену не ФАГ, а інших ферментів, так звані ФКУ2, ФКУ3 и ФКУ4. Ці захворювання лікуються інакше, але одразу їх розпізнати практично неможливо.
Тому ми в своїй роботі форму захворювання оцінюємо через кілька місяців після початку лікування, а остаточно – в 1 рік з врахуванням стану розвитку хворого, динаміки рівня ФА. В нашій практиці був випадок атипової форми захворювання, очевидно, ФКУ3.
Крім ФКУ є ще стан, який називають гіперфенілаланінемією (ГФА), коли рівень ФА не перевищує 10 мг%. Рішення про призначення дієтотерапії приймається індивідуально для кожної дитини, хоча найчастіше, застосування білкових гідролізатів не є необхідним.
В сім’ях, де є хворі на ФКУ, проводиться медико-генетичне консультування та молекулярно-генетичне обслідування з метою ідентифікації мутації гену, що викликав захворювання. При повторній вагітності проводиться пренатальна діагностика ФКУ у плода.
Номер з каталогу МІМ:
261600 Phenylketonuria; PKU
Переглянуто редакційною колегією I.B.I.S.: 15/02/2002
Дивіться також:
- Продукти з низьким вмістом фенілаланіну
- Низькобілкові продукти харчування (ФКУ) виробництва Польщі
- Кулінарні рецепти для осіб з низькофенілаланіновою дієтою
- З досвіду лікування фенілкетонурії при пізній діагностиці в Одеському ММГЦ
- Фенілкетонурія (інформація для спеціалістів)
- Фенілкетонурія (інформація для батьків)
Викидень
(Miscarriage)
Ірина Харитонова
Координатор Українського Альянсу
із запобігання вродженим вадам розвитку
Викидень – це дуже сумний та жахливий досвід. Вагітність, яка, здавалося проходила нормально, раптово обривається, лишаючи батьків спустошеними. Ця трагедія трапляється у 15-20% всіх випадків вагітності.
Викиднем називається втрата вагітності у термін до 20 тижнів, ще до того як плід здатний вижити поза маткою. Більшість викиднів трапляються у першому триместрі (перші 12 тижнів вагітності). Деякі лікарі вважають, що до 50% всіх вагітностей закінчуються викиднем, ще до того як жінка впевнилася, що вона вагітна.
Чому трапляються викидні?
Причина викиднів цілком ще не з’ясована. Коли у жінки трапляється викидень у першому триместрі, лікар часто не може встановити причину. Однак більшість викиднів трапляється при неправильному перебігу вагітності. Звичайно ні жінка, ні лікар нічого не можуть зробити, щоб запобігти цьому.
Чинники, що викликають викидні першого триместра вагітності відомі. Перш за все – це хромосомні аномалії плоду. Хромосоми – це крихітні ниткоподібні утворення, що є у кожній клітині організму і що містять наші гени, які обумовлюють всі наші характерні ознаки від кольору очей до дії наших внутрішніх органів. Кожна особа має 23 пари хромосом (всього 46). Пара складається з однієї хромосоми від матері і однієї від батька. До 70% всіх викиднів першого триместру вагітності трапляється через хромосомні аномалії плоду.
Більшість хромосомних аномалій є результатом ушкодження яйцеклітини чи сперматозоїда. До настання вагітності яйцеклітина і сперматозоїд поділяються, щоб утворити клітини з 23 хромосомами. Деколи хромосоми з яйцеклітин та сперматозоїдів розходяться неоднаково, чи на одну більше, чи на декілька меньше. Коли вагітність настає за участю яйцеклітини чи сперматозоїда з помилковим набором хромосом, у зародка формується хромосомна аномалія. Ці зародки часто не виживають, трапляється викидень. З віком у жінок хромосомні аномалії виникають все частіше, ось чому жінки старші 35 років мають більший ризик викидня ніж молодші за віком жінки.
Хромосомні аномалії можуть також викликати загибель зрілої яйцеклітини. В таких випадках плодові оболонки можуть зовсім не містити плід, чи тому що зародок не сформувався, чи тому що його розвиток припинився дуже рано. На ранніх етапах вагітності жінка може помітити, що симптоми вагітності у неї припинилися, а з’явилися темно-коричневі виділення з піхви. Проведене ультразвукове обстеження покаже, що плодові оболонки порожні. Загибель зрілої яйцеклітини зрештою закінчується викиднем, однак викидень може тривати протягом тижнів. Оскільки очікування викидня є психологічно важким, часто лікарі пропонують процедуру вишкрябування матки.
У більшості випадків, коли у жінки трапляється викидень у першому триместрі вагітності, лікар назве як більш імовірну причину хромосомні аномалії. Однак інші чинники також можуть спричиняти викидні першого триместру. Це можуть бути гормональні розлади, інфекції та загострення хронічних захворювань у матері.
Спосіб життя матері також може підвищити ризик викидня у першому триместрі вагітності. Дослідження показали, що жінки які вживають алкогольні напої два чи більше разів на день, вдвічі підвищують ризик мати викидні. У жінок, які палять цигарки, ризик мати викидень на 20-80% вищий за ризик, що його мають не курці. Деякі дослідження також свідчать, що жінки, які вживають три чи більше чашки кави на день (або еквівалентну кількість кофеїну) також мають підвищений ризик.
Викидні другого триместру вагітності частіше пов’язані з проблемами будови матки, як, наприклад, аномалії розвитку чи слабка шийка матки, що передчасно розкривається. Так саме як і у першому триместрі, до викиднів можуть призвести інфекції матері та хромосомні аномалії. На хромосомні аномалії припадає до 20% викиднів другого триместру вагітності. Певні проблеми з боку імунної системи також можуть спричинити викидень.
Сексуальні стосунки, фізичні вправи чи помірна робота на присадибній ділянці (без контакту з отрутохімікатами та пестицидами) не бувають причиною викиднів.
Які обстеження треба пройти після викидня?
Після першого викидня у першому триместрі лікарі звичайно не призначають ніяких обстежень. Причина цих ранніх втрат часто невідома. Деякі спеціалісти пропонують обстеження тканин плода (абортуса) на підтвердження наявності хромосомних аномалій, що призвели до викидня.
Якщо у жінки трапився викидень у другому триместрі, лікарі часто можуть встановити причину. Для цього лікар запропонує провести деякі аналізи, включно аналіз крові.
Що є причиною повторних викиднів?
Звичайно викидень є поодиноким явищем, однак кожна двадцята подружня пара має два викидні підряд (один за одним), а три і більше викиднів трапляються у співвідношенні 1:100. Жінки, які мали два чи більше викидня, повинні пройти повне медичне обстеження, щоб встановити причину викиднів і що потрібно зробити щоб запобігти цьому. Принаймні у 70% подружніх пар обстеження можуть встановити причину викиднів, що повторюються.
В даний час лікарі мають значно більше інформації про те, чому саме у деяких пар виникають повторні викидні і як запобігти цьому. Ось деякі з найбільш поширених причин:
- Хромосомні порушення. Раніше вважалося, що хромосомні порушення звичайно виникають тільки один раз, однак останні дослідження показали, що до 60% всіх повторних викиднів можуть бути викликані саме порушеннями хромосомного апарату. У більшості батьків, які зазнали повторних викиднів, хромосоми є нормальними, однак існує 5% імовірность наявності хромосомної перебудови у партнера, що не впливає на його/її стан здоров’я, але може спричинити хромосомні порушення у плода, а результатом цього буде викидень. Для перевірки на хромосомні перебудови (поломки) рекомендується провести аналіз крові на каріотипування.
- Порушення з боку матки. 15-30% всіх повторних викиднів можуть статися через аномалії розвитку матки. Такі викидні трапляються в першому та другому триместрі. У деяких жінок від народження матка буває замалою, має неправильну форму, повні чи часткові перетинки. У інших утворюються доброякісні пухлини (фіброми) чи рубці від минулих операцій. Це обмежує простір, що є необхідним для зростаючого плоду, і заважає матковому кровообігу. Порушення з боку матки виявляються декількома методами огляду матки, включно ультразвукове обстеження, рентгенографію матки чи гістероскопію (огляд матки через спеціальний оптичний прилад, що вводиться через шийку матки). Багато аномалій можна виправити хірургічним шляхом, деколи навіть під час діагностичної процедури, що значно покращує перспективу майбутньої вагітності. Слабка шийка матки (недостатність шийки) чи тіло матки можуть призвести до викидня звичайно у терміні 16-18 тижнів вагітності. Повторних викиднів, що спричинені недостатністю шийки, можна запобігти, якщо на ранніх етапах наступної вагітності на шийку накласти шов.
- Ендокринні розлади. Ризик викиднів зростає, коли ендокринні залози виробляють занадто багато чи занадто мало відповідного гормону. Низькі рівні гормону прогестерону, що грає ключову роль на ранніх етапах вагітності, викликають від 15 до 60% втрат до 10 тижнів вагітності. У жінок з низьким рівнем прогестерону, що повторюється від одного менструального циклу до другого, можна говорити про дефект лютеїнової фази. Діагноз ставиться за допомогою ендометріальної біопсії (для встановлення рівня прогестерону забирається маленький шматочок внутрішнього шару тканини матки) чи повторних досліджень крові. Лікування синтетичними гормональними препаратами чи натуральним прогестероном у вагінальних кульках часто допомагає запобігти наступним викидням.
- Порушення імунного захисту. В організмі людини виробляються білки, так звані антитіла, що борються з інфекціями, але при деяких станах виникають білки, що звуться аутоантитіла, які можуть атакувати свої власні тканини, що спричиняє безліч проблем. Конкретні типи аутоантитіл, такі як антикардіоліпін, спричиняють виникнення кров’яних згустків, що можуть перешкоджати протіканню крові по судинах плаценти. Дослідження показують, що ці та схожі з ними антитіла, що мають назву антифосфоліпідні антитіла, є причиною 5-15% повторних викиднів. Спеціальні аналізи крові можуть визначити їхній рівень. Лікування постраждалих жінок малими дозами аспірину та гепарину (препарат, що робить кров рідшою) у 70-80% закінчується народженням здорової дитини. Вчені досліджують чи можуть інші стани порушень імунної системи бути причиною того, що організм жінки сприймає власний плід як чужорідну тканину.
- Інфекції та інші чинники. У виникненні повторних викиднів також відіграють роль деякі безсимптомні інфекції статевих шляхів. Якщо діагностована інфекційна хвороба, подружня пара буде пролікована антибіотиками до настання вагітності. Контакт на робочому місці з промисловими розчинниками вагітної жінки чи її партнера може деколи призвести до викидня. Перелік контактних хімікатів має бути обговореним з лікарем.
У 25% випадків причину повторних викиднів встановити неможливо. Однак за цих обставин не треба втрачати надію: 60% жінок, які мали повторні викидні, навіть без лікування зрештою мають здорову вагітність.
Скільки часу триває одужання після викидня?
Фізичне одужання триває місяць чи більше, залежно від терміну вагітності. Деякі гормони вагітності залишаються в крові ще один-два місяці після вагітності. У більшості жінок менструальний цикл відновлюється через чотири-шість тижнів після викидня.
Значно більше часу триває емоційне одужання. Жінки та їх партнери можуть зазнавати великого горя від цієї втрати. Жінка може відчувати заціпеніння, сум, провину, труднощі зосередитись, депресію та лють. Він та вона можуть переживати своє горе різними шляхами, створюючи напруження у взаєминах в той час, коли вони більш за все потрібні один одному. Не треба цуратися запитати свого лікаря чи може він знає порадника, який має досвід у втратах вагітності. Багатьом парам допомагають групи психологічної підтримки, де вони можуть поділитися своїми почуттями з іншими, хто також втратив вагітність.
Через який час після викидня жінка може робити спробу завагітніти?
Жінці не потрібно робити спробу завагітніти поки вона повністю фізично та емоційно не буде підготовленою до цього. З медичної точки зору, якщо жінка не проходить спеціальних досліджень чи лікування, треба зачекати відновлення хоч одного нормального менструального циклу.
Однак може пройти значно більше часу поки жінка відчує себе морально підготовленою до наступної вагітності. Тільки вона може сказати, коли втихне її горе і вона буде готовою до очікування іншої дитини.
Багатьох жінок, які пройшли через таке випробування турбує, що вони знову втратять дитину. На щастя, принаймні 85% жінок, які мали один викидень, у подальшому мали здорову вагітність, а у разі двох чи більше викиднів ця цифра становить 75%.
Взагалі жінкам було б добре проконсультуватись із спеціалістом ще до того, як вони завагітніють. Якщо у жінки було два чи більше викиднів, а особливо якщо вона старша 35 років, або якщо вона хвора на діабет чи системний червоний вовчак, це може негативно відбитися на вагітності чи на заплідненні. В цьому разі їй потрібно звернутися до спеціаліста, досвідченого у перебігу вагітностей з високим ризиком. Дільничний спеціаліст порадить відповідного фахівця, який порекомендує які саме обстеження необхідно пройти перед настанням іншої вагітності, таким чином щоб жінка отримала найкраще лікування для підвищення шансів мати наступну здорову вагітність.