Фенілкетонурія
(Phenylketonuria, PKU)
Любов Степанівна Євтушок
Зав. медико-генетичною консультацією
Рівненського клінічного лікувально-діагностичного центру
Фенілкетонурія – це спадкове захворювання, яке, при відсутності лікування призводить до розумової відсталості. 1 з 50-70 людей є носієм гена фенілкетонурії. Хоча ця хвороба не дуже поширена (1 дитина на кожних 8-13 тисяч новонароджених), вона потребує великих витрат. В США, наприклад, щороку витрачається кілька мільйонів доларів на лікування хворих дітей. Але навіть це не можна порівняти з тим горем, яке приходить в сім‘ю з народженням хворої дитини.
Фенілкетонурія – це спадкова хвороба, яка зумовлена дефектом гена ферменту фенілаланінгідроксилази, що знаходиться на довгому плечі 12 хромосоми (12q 22-24). Саме це і призводить до порушення обміну амінокислоти фенілаланіну – необхідної для життя амінокислоти, яку ми отримуємо з їжі.
“Феніл” – від слова фенілаланін (назва однієї з 20 амінокислот, які входять у склад білкової молекули).
“Кетон” – від слова кетони (продукти обміну цієї амінокислоти).
“Урія” – виділення продуктів обміну з сечею.
Порушення метаболізму фенілаланіну:
В нормі фенілаланін перетворюється на тирозин за допомогою ферменту гідроксилази фенілаланіну (ФФГ). Для цього перетворення необхідний тетрагідробіоптерин (ВН4). Він необхідний також для біохімічних процесів в ході синтезу нейромедіаторів – допаміну, норепінефріну, і серотоніну. В нормі рівень фенілаланіну в крові відповідає 180 mmol/l (3 mg/dl) або менше.
Причини підвищення рівня феніаланіну:
Існує кілька причин підвищення рівня фенілаланіну в крові (гіперфенілаланінанемія) (табл. 1). Тому, це відхилення потребує детального дослідження перед тим, як встановлювати конкретний діагноз для немовляти з гіперфенілаланінамією та призначати лікування. Нижче поданий перелік причин гіперфенілаланінамії та біохімічні показники для їх диференціації.
Таблиця 1.
Причини підвищення фенілаланіну.
|
Фенілкетонурія (ФКУ)
|
>1200
|
<250
|
Норма
|
Норма
|
Норма
|
|
ФКУ середньої важкості
|
600 – 1.200
|
<250
|
Норма
|
Норма
|
Норма
|
|
Гіперфенілаланінемія, не пов’язана із ФКУ
|
180 – 600
|
<250
|
Норма
|
Норма
|
Норма
|
|
Дефекти птерину
|
|||||
|
Дефіцит циклогідролази
|
180 – 1.200
|
<250
|
Норма
|
Аномальний
|
Аномальний
|
|
Дефіцит синтезу пірувол -тетрагідроптеріну
|
180 – 1.200
|
<250
|
Норма
|
Аномальний
|
Аномальний
|
|
Дефіцит дегідроптерін-редуктази
|
180 – 1.200
|
<250
|
Норма
|
Аномальний
|
Аномальний
|
|
Транзиторна гіперфенілаланінемія
|
180 – 840
|
<250
|
Норма
|
Норма
|
Норма
|
|
Тирозинемія І, галактоземія, хвороби печінки
|
180 – 600
|
>250
|
Підвищений рівень метіоніну
|
Норма
|
Норма
|
Дефіцит гідроксилази фенілаланіну:
Дефіцит активності ФФГ призводить до підвищення рівня фенілаланіну в крові. Ступінь підвищення залежить від ступеня ензимної недостатності. Класична форма ФКУ, яка в Сполучених Штатах та Європі трапляється з частотою 1:13.000, зазвичай дає при обстеженні такі показники: 1) концентрація фенілаланіну в крові 1200 mmol/l (20 mg/dl) і вище у новонароджених при грудному вигодуванні або вживанні суміші; 2) концентрація тирозину в крові менше 250 mmol/l (5 mg/dl); 3) проба на птерин у сечі, який вказує на недостатність ВН4, в нормі. При класичній формі ФКУ активність ФФГ печінки наближається до нуля. При м’яких формах ФКУ (атипова ФКУ) спостерігається рівень фенілаланніну в крові у межах 600-1200 mmol/l (10-20 mg/dl), нормальний або низький рівень тирозину, нормальна проба на птерин у сечі; на цьому фоні проявляється незначна резидуальна/залишкова активність ФФГ.
Приблизно 20-50% немовлят, у яких була виявлена гіперфенілаланінанемія під час скрінінгу новонароджених, мали стійку м’яко виявлену, не пов’язану з ФКУ гіперфенілаланінанемію (МГФ) з рівнем фенілаланіну в крові 180-600 mmol/l (3-10 mg/dl) та стійкою активністю ФФГ до 10%. МФГ вважалась не шкідливою, але, грунтуючись на результатах останніх досліджень, було висунуто припущення, що стійке підвищення фенілаланіну в крові вище 360 mmol/l (6mg/dl) може знижувати показник розумового розвитку IQ. Інші дослідження, навпаки, показують, що стійке підвищення фенілаланіну в крові до рівня 600 mmol/l (10mg/dl) не викликає ніяких проблем. Існує розбіжність в поглядах на те, чи призначати обмежуючу дієту немовлятам з рівнем фенілаланіну 360-600 mmol/l (6-10 mg/dl). У деяких клініках дієтичне лікування призначається дітям з рівнем фенілаланіну вище 480 mmol/l (8mg/dl).
Порушення, пов’язані з тетрагідробіоптеріном:
Порушення синтезу та переробки ВН4 призводять до виникнення гіперфенілаланінанемії. Важливо відмітити, що діти з цим відхиленням страждають на прогресуючу, часто у важкій формі, неврологічну деградацію, якщо їм помилково ставлять діагноз класичної ФКУ і лікують тільки дієтою із зниженим вмістом фенілаланіну. Недостатність ВН4 обмежує перетворення фенілаланіну на тирозин, а пов’язане з діяльністю ЦНС перетворення тирозину в DOPA та триптофану в 5-гідрокситриптофан. Таким чином, ці порушення призводять до підвищення фенілаланіну та порушень у синтезі нейромедіаторів. Рідко трапляються випадки, коли недостатність ВН4 є тільки периферійною і не впливає на синтез медіаторів в ЦНС, де їх рівень залишається в нормі. За останні роки в деяких країнах був налагоджений збір даних з діагностики та лікування цього рідкісного захворювання (1:1.000.000 або 1% від усіх новонароджених з неонатальною гіперфенілаланінанемією). Лікування передбачає введення додаткового ВН4 і медикаментів, які підвищують рівень нейромедіаторів.
Транзиторна гіперфенілаланінанемія:
Гіперфенілаланінанемія, виявлена під час скрінінгу новонароджених, може мати тимчасовий характер. Це, як правило, відносно невисоке підвищення фенілаланіну, що спостерігається у перші місяці життя і не потребує спеціальної терапії. У деяких випадках гіперфенілаланінанемія є вторинною як наслідок тимчасової гіпертирозинанемії. Описані випадки більш важких форм тимчасової гіперфенілаланінанемії, при яких спочатку виникала необхідність в лікуванні (рівень 480-840 mmol/l або 8-18 mg/dl). Згодом видужання наставало само по собі в процесі росту дитини. На малюнку 1 показано алгоритм лікування при неонатальній гіпераланінемії.
Малюнок 1.
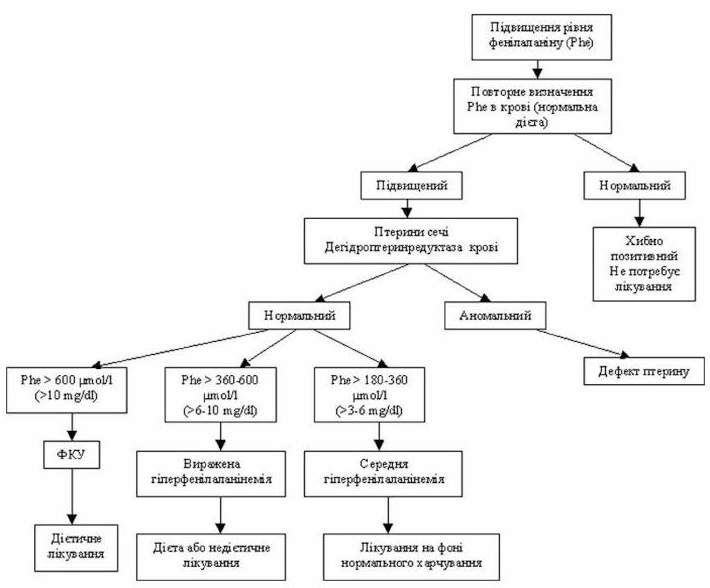
Тирозинемія І-го типу (спадкова тирозинемія):
Гіперфенілаланінанемія часто трапляється при тирозинемії І-го типу. Це симптом вторинного характеру. Очевидно, він виникає внаслідок важкого метаболічного ураження печінки. Одночасне визначення рівнів фенілаланіну та тирозину дає змогу визначити результатом тирозинемії чи ФКУ є гіперфенілаланінанемія.
Галактоземія та інші захворювання:
Галактоземія та інші захворювання, які викликають дисфункцію печінки, також можуть спричинити підвищення фенілаланіну в крові вторинного характеру. У таких випадках гіперфенілаланінанемія супроводжується підвищенням в крові рівня метіоніну та тирозину. Щоб виявити такі вторинні причини гіперфенілаланінанемії, необхідно провести подальше обстеження дитини та знати її клінічний фенотип.
Як це впливає на дитину?
Внаслідок порушення обміну фенілаланін накопичується в крові і тканинах і стає “отрутою” для організму дитини, що росте.
Діти, які народилися з фенілкетонурією, в перші кілька місяців здаються цілком здоровими. Але, якщо лікування не розпочате, вони через 3-5 місяців втрачають набуті навички, інтерес до оточення. А коли їм виповнюється рік, вони вже мають розумову відсталість.
Діти з ФКУ мають знижений м’язовий тонус, часто є дратівливими. Їх тіло і сеча мають характерний мишачий запах або запах плісняви. Шкіра у них буває суха, часті дерматити. В деяких випадках виникають судоми, характерні “кивки”. Як правило, хворі діти добре розвиваються фізично, мають надмірну вагу і світліше волосся, ніж їх родичі.
Генетика ФКУ (яким чином передається ця хвороба?)
Фенілкетонурія є спадковою хворобою. Вона проявляється лише тоді, коли обидва батьки мають ген хвороби і передають його дитині. Такий тип успадкування називається аутосомно – рецесивним. Якщо в одній клітині є один нормальний ген і один ген фенілкетонурії, то така людина називається носієм. Вона не має ніяких проявів хвороби, але може передати хворобливий ген своїм нащадкам (Схема № 1).
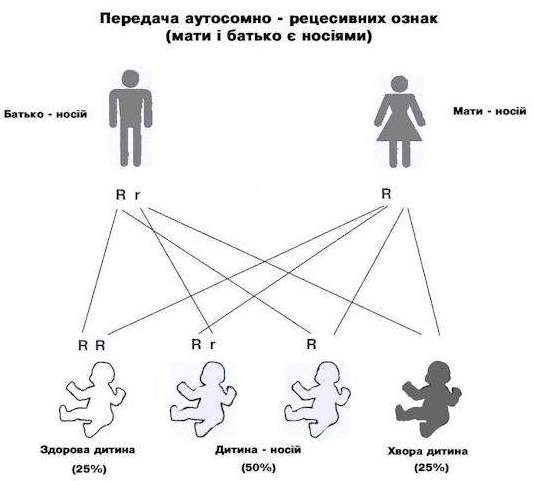 Схема № 1.
Схема № 1.
Якщо обидва батьки є носіями, то існує 25% шансів, що кожен з них передасть дефектний ген дитині, викликаючи таким чином народження хворої дитини. Є також 25% шансів (1 з 4), що вони передадуть здорові гени і дитина народиться цілком здоровою. І, нарешті, є 50% шансів, що у дитини буде один нормальний ген і один ген фенілкетонурії. В цьому випадку дитина буде носієм, як і її батьки.
Чи є можливість діагностувати ФКУ?
Так. За допомогою спеціального тестування крові (потрібно лише кілька крапель, які висушують на фільтрувальному папері) можна діагностувати хворобу, коли дитина має лише 5-6 днів від народження і знаходиться в пологовому будинку. Проби крові аналізуються на рівень фенілаланіну і визначається причина його підвищення, якщо таке є.
Помилково позитивні результати скрінінгу новонароджених – це тимчасові відхилення від норми, причиною яких є не порушення обміну речовин, а інші фактори, наприклад, недоношеність. Вони викликають в сім’ях тривогу. Щоб полегшити переживання батьків, необхідно пояснити їм результати аналізів та необхідність проведення повторного обстеження.
Існує також тест сечі з трихлорним залізом, але він дає менш надійні результати. Причина полягає в тому, що в перші дні життя фенілаланін не може накопичуватись на рівнях, які необхідні для отримання позитивного результату тесту.
Молекулярна діагностика (діагностика на рівні гена) можлива як для пренатальної (допологової), так і постнатальної (післяпологової) діагностики хвороби.
Обстеження дитини з фенілкетонурією:
Обстеження дитини з ФКУ включає встановлення кількісних рівнів амінокислот в плазмі та сироватці при особливій увазі до фенілаланіну та тирозину, а також збір проб крові та сечі на аналіз птеріну. Паралельно з цим батьків інформують про особливості ФКУ та подібних захворювань та надають консультацію з генетичних питань. У деяких випадках, особливо коли необхідність введення дієти стає більш нагальною, ніж видавалось після перших аналізів, доцільно зробити аналіз на ФФГ – генотип, щоб переконати батьків в точності діагнозу і в необхідності тривалого медичного нагляду. Визначення рівня фенілаланіну в крові кожного з батьків повинно бути зроблене на початку обстеження дитини. Рідко трапляється так, що у когось з батьків підвищений рівень фенілаланіну.
Лікування фенілкетонурії:
З того моменту, як обстеження показало, що рівень фенілаланіну у дитини вимагає розпочати лікування (в багатьох клініках це 480 mmol/l або 8mg/dl), вводиться дієта з обмеженим вмістом фенілаланіну. Якщо аналізи на птерин показали відхилення від норми, може виникнути потреба в додатковому прийомі ВН4 та медикаментів, які збільшують рівень нейромедіаторів.
Принцип лікування фенілкетонурії – спеціальна дієта, тобто лікувальне харчування. Він полягає в обмеженні поступлення в організм дитини фенілаланіну з їжею. Якщо розпочати дієту з 10 – 20-го дня життя, то це запобігає розвитку розумової відсталості.
Фенілаланін входить у склад всіх білкових продуктів. Тому із раціону харчування хворого необхідно виключити ті продукти, які мають багато білка. До них відносяться м‘ясо, риба, яйця, молоко та молочні вироби, хліб.
Лікувальне меню хворого, в основному, складають продукти рослинного походження – овочі, фрукти, ягоди, зелень. Але організм дитини не може формуватися при такому дефіциті білка. Тому в раціон дитини додають спеціальні лікувальні суміші, в складі яких зменшена кількість або повністю видалений фенілаланін, такі як Лофеналак, Феніл-фрі, Нофелан та інші.
Розрахунок білкового компоненту їжі для хворої дитини повинен робити лікар.
Період грудного віку:
Кожне годування розпочинається з пляшечки з амінокислотним додатком. Після того, як прорахована необхідна кількість рідини випита, дитина отримує важливий для життя фенілаланін з грудного молока матері. При ФКУ споживається невелика кількість натуральної їжі. Грудне молоко містить відносно малу кількість фенілаланіну і є найбільш адаптованим для немовляти, тому мам заохочують до грудного вигодовування. Якщо жінка не вигодовує дитину грудним молоком, дитині дають невелику кількість суміші додатково до амінокислотної добавки. У процесі росту дитини дієта доповнюється крупами без вмісту протеїну і точно виваженою кількістю овочів та фруктів. З ростом дитини і розширенням її раціону, батьки матимуть час дізнатись, як поступово ускладнювати дієту.
Щоденна необхідність вживати амінокислотні добавки крім звичайної їжі може стати причиною конфлікту і призвести до відчаю, злості, сліз, як у дітей, так і у батьків.
Схема введення продуктів прикорму для грудної дитини така ж, як і у здорових. Спочатку вводяться соки, потім фруктове і овочеве пюре. В раціоні хворої дитини необхідна сагова каша або безбілкова крупа. З віком раціон розширюється (вегетаріанські страви, безбілковий хліб).
Дитинство та підлітковий вік:
Діти та підлітки з ФКУ вважають, що для них вибір їжі дуже обмежений. Менших дітей вчать нічого не їсти і навіть не пробувати без дозволу батьків. Звичайну їжу необхідно точно зважувати до грама і складати меню на день. Три або чотири рази на день треба вживати амінокислотні добавки до їжі. Із вживанням добавок проблем у більшості випадків не виникає, за виключенням тих випадків, коли хворий негативно реагує на їх смак чи запах. Важливо, щоб усі, хто спілкується з дитиною, знали про ФКУ достатньо для того, щоб не дати дитині не ту їжу або не в тій кількості. Важливо також проінформувати друзів та родичів, вихователів у дитсадку, осіб у школі, які відповідають за догляд за дитиною.
Амінокислотні добавки, розрахунок дієти, спеціальні продукти без вмісту протеїну необхідно мати з собою на усіх виїздах та в подорожах. На ринку починають з’являтись нові форми, альтернативні амінокислотним добавкам у порошку. У спресовану вигляді чи в капсулах вони займають менше місця, і можуть вживатись додатково або замість порошку під час подорожей або на вечірках.
Оскільки дотримання дієти має бути дуже суворим і пов’язане з великою кількістю розрахунків та вимірів ваги, у батьків та дітей з ФКУ часто розвивається сильне відчуття взаємозалежності. Важливо навчати дітей та підлітків усьому, що пов’язане з їхнім станом, щоб вони поступово ставали більш обізнаними і здатними самостійно давати собі раду. Перед сім’єю та найближчим оточенням дитини стоїть завдання забезпечити такі умови, при яких дитина виросте незалежною та розвине у собі нормальну самооцінку.
ФКУ є непомітною інвалідністю. При порушенні дієти недуга проявиться з новою силою через деякий час. Необхідно надати інформацію вчителям, які ведуть уроки кулінарії у школі. Дітям, хворим на ФКУ, необхідно дати можливість отримати практичні знання з самостійного приготування спеціальної їжі.
Дівчаток-підлітків з ФКУ необхідно рано проінформувати про контрацепцію. Особливо сувора дієта є необхідною як перед, так і під час вагітності. Вагітність необхідно планувати.
ФКУ сама по собі не впливає на вибір навчального закладу. Однак, якщо навчання чи майбутня професія будуть такими, при яких важко дотримуватись дієти, рекомендується від них відмовитись. Хворих на ФКУ звільняють від проходження військової служби через необхідність спеціальної дієти.
Дорослі з ФКУ:
Батьки повинні усвідомлювати свою велику відповідальність і забезпечити умови існування, при яких дитина залишатиметься здоровою. Необхідно ретельно виконувати рекомендації по дієтлікуванню дитини, щоб забезпечити її нормальний розвиток.
До недавнього часу діти з ФКУ отримували лікування обмежуючою дієтою тільки в дошкільний період, оскільки вважалось, що з настанням шкільного віку розвиток мозку припиняється, і загроза його ушкодження через надлишок фенілаланіну минає. Однак останні дослідження показують, що багато дітей, які припинили дієтотерапію, мають нижчий показник IQ і гірші показники в навчанні, ніж ті, що залишились на спеціальній дієті. В деяких дослідженнях описані випадки неврологічних порушень, аномалій мозкової діяльності, що впливають на уяву, проблеми психічного характеру у пацієнтів, які припинили дієту в ранньому шкільному віці і ніколи не перебували під належним наглядом спеціалістів з метаболічних захворювань. Виходячи з цього, хворим на ФКУ рекомендовано залишатись на обмежуючій дієті протягом усього життя та регулярно проходити на належному рівні огляд з приводу метаболічних захворювань.
Хоча рівень фенілаланіну, який рекомендують підтримувати, та частота проведення аналізів крові можуть відрізнятись у різних клініках, існують стандартизовані інструкції з дієти при захворюванні на ФКУ, розроблені британськими лікарями. Вони рекомендують розпочинати дієтотерапію не пізніше, ніж протягом перших 20-ти днів життя для усіх немовлят, в яких рівень фенілаланіну постійно становить вище 400 mmol/l (6.7mg/dl), підтримувати фенілаланін на рівні 120-360 mmol/l (2-6 mg/dl) в ранньому дитинстві та на рівні 480 mmol/l (8 mg/dl) у шкільному віці. Усвідомлюючи те, що, з ростом дитини з дотриманням суворої дієти виникають труднощі, пропонується підтримувати фенілаланін на рівні не вище 700 mmol/l (12 mg/dl), але навіть при такій концентрації у підлітків і дорослих виникають труднощі розумового плану в прийнятті рішень.
Дослідження у Норвегії та інших країнах показали, що сувора дієта має позитивний вплив і на тих дорослих, які ніколи до цього не лікувались від ФКУ.
Кількість дорослих молодих людей, які проходять лікування з раннього дитинства, зростає. Деякі з них дотримуються дієтичного харчування, інші – споживають звичайну їжу відповідно до тих рекомендацій, які існували до середини 80-их років. Є також такі, хто повернувся до дієти після різних за часом періодів звичайного харчування. Хворі, які обрали дієтичне лікування, зазначають, що їх стан покращується, коли вони утримують низький рівень сироваткового фенілаланіну.
ФКУ не є обмеженням для шлюбу, спільного проживання, сімейного життя. Але молоді люди повинні усвідомлювати, що їх діти будуть носіями гена ФКУ. Це не означає, що вони обов’язково захворіють на ФКУ, оскільки захворювання передається від обох батьків.
Контроль за лікуванням:
Правильність дієтлікування ФКУ підтверджується визначенням рівня фенілаланіну в крові. На фоні дієтлікування він не перевищує 4-8 мг%.
Частота проведення моніторингу крові теж різна, але британські медики рекомендують робити аналізи щотижня для дітей до 4-х років, кожні 2 тижні для дітей 4-10-ти років і щомісяця після 10-ти років. У деяких клініках прийнятий менш напружений графік моніторингу. Зазвичай, немовлята проходять обстеження щотижня поки рівень фенілаланіну в них не знизиться до 120-360 mmol/l (2-6 mg/dl). Після цього вони здають аналізи щотижня протягом перших 6-ти місяців життя, раз у два місяці – до 1 року життя, кожні 3-4 місяці – до 5-ти років і раз у півроку – на протязі усього життя. Рівень фенілаланіну визначається щотижня за допомогою аналізів крові, взятої батьками з проколу в пальчику дитини і висушеної на фільтрувальному папері. Старші діти, підлітки та дорослі теж беруть пробу крові самі у себе з проколу в пальці.
Контроль за лікуванням, фізичним та розумовим розвитком дитини здійснюють лікар-генетик, дитячий психіатр, психолог. У періоди частих інфекційних захворювань може виникнути потреба частіше перевіряти рівень фенілаланіну в сироватці крові.
Щеплення дітям проводять за звичайним графіком.
Материнство і ФКУ:
Коли жінка з фенілкетонурією вагітніє, існує високий ризик мікроцефалії, вроджених вад серця, розумової відсталості у її дитини, бо мозок ще ненародженої дитини пошкоджується ненормальним обміном речовин матері. Було відмічено високий показник спонтанних абортів.
Однак розумовій відсталості дитини можна запобігти. Дуже важливо майбутній матері знову розпочати дієтлікування і контролювати рівень фенілаланіну в крові перед зачаттям і в період вагітності щотижня. Дівчина – підліток повинна готуватися до майбутнього дорослого життя завчасно.
Дані літератури свідчать, що при дотриманні дієти та компетентному біохімічному контролі для підтримання рівня фенілаланіну на показниках 120-360 mmol/l протягом вагітності, народжуються здорові діти.
Номер з каталогу МІМ:
261600 Phenylketonuria; PKU.
Література:
- Frances E. Dougherty, Harvey L. Levy. “Phenylketonuria”. Devision of Genetics, Children’s Hospital and Department of Pediatrics, Harvard Medical School, Boston, MA 02115, USA.- Annales Nestle 1998, 56: 83-93.
- William L. Nyhan, M.D., Ph.D., Nadia A. Sakati, M.D. “Diagnostic Recognition of Genetic Disease”. Lea & Febiger, Philadelphia, 1987, 100-105.
Переглянуто редакційною колегією I.B.I.S.: 05/02/2004
Дивіться також:
- Продукти з низьким вмістом фенілаланіну
- Низькобілкові продукти харчування (ФКУ) виробництва Польщі
- Кулінарні рецепти для осіб з низькофенілаланіновою дієтою
- Досвід діагностики та лікування хворих на фенілкетонурію, виявлених по програмі скринінгу
- З досвіду лікування фенілкетонурії при пізній діагностиці в Одеському ММГЦ
- Фенілкетонурія (інформація для батьків)







